Содержание страницы
1. Безопасность пищевых продуктов
Проблема безопасности продуктов питания — сложная комплексная проблема, требующая многочисленных усилий для ее решения, как со стороны ученых — биохимиков, микробиологов, токсикологов и др., так и со стороны производителей, санитарно-эпидемиологических служб, государственных органов и, наконец, потребителей.
Актуальность проблемы безопасности продуктов питания с каждым годом возрастает, поскольку именно обеспечение безопасности продовольственного сырья и продуктов питания является одним из основных факторов, определяющих здоровье людей и сохранение генофонда.
Под безопасностью продуктов питания следует понимать отсутствие опасности для здоровья человека при их употреблении, как с точки зрения острого негативного воздействия (пищевые отравления и пищевые инфекции), так и с точки зрения опасности отдаленных последствий (канцерогенное, мутагенное и тератогенное действие). Иными словами, безопасными можно считать продукты питания, не оказывающие вредного, неблагоприятного воздействия на здоровье настоящего и будущих поколений.
2. Классификация чужеродных веществ и пути их поступления в продукты
Чужеродные химические вещества (ЧХВ) могут попадать в пищу случайно в виде контаминантов — загрязнителей, например, из окружающей среды или в процессе технологической обработки при контакте с оборудованием; иногда их вводят специально в виде пищевых добавок, когда это связано с технологической необходимостью. Кроме того, в пищевом сырье и готовых продуктах питания могут содержаться природные компоненты, оказывающие вредное влияние на здоровье человека.
В целом, классификация вредных и посторонних веществ в сырье, питьевой воде и продуктах, питания может быть представлена в виде схемы (см. рис. 1).
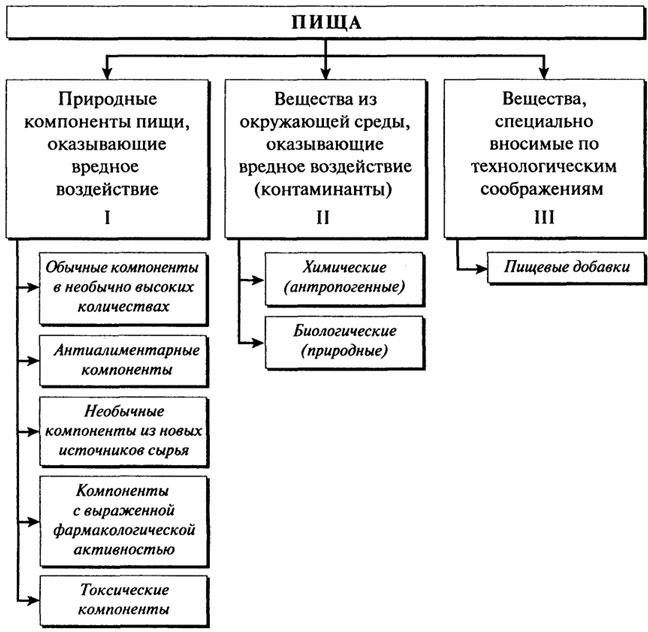
Рис. 1. Классификация посторонних и вредных веществ пищи
Несмотря на то, что окружающая среда остается главным источником загрязнения сырья и пищевых продуктов, в настоящее время появляются новые и модифицируются традиционные технологии получения продуктов питания, которые часто связаны с применением жестких видов воздействия на сырье и полупродукты, что, в свою очередь, является не всегда оправданным и приводит в возникновению токсичных веществ.
Кроме того, получили широкое распространение разнообразные виды непроверенных пищевых добавок и новых упаковочных материалов; появилось большое число малых предприятий, технологический процесс и качество выпускаемых продуктов питания на которых плохо контролируется или вообще не контролируется.
Нельзя забывать и об антиалиментарных факторах питания, содержащихся в сырье и готовых пищевых продуктах и способных оказывать неблагоприятное воздействие на организм человека.
3. Источники загрязнения сырья и пищевых продуктов
1. Окружающая среда – основной источник загрязнения сырья и пищевых продуктов. Загрязнение продовольственного сырья и пищевых продуктов чужеродными веществами или ксенобиотиками напрямую зависит от степени загрязнения окружающей среды.
В результате хозяйственной деятельности человека в биосфере циркулирует огромное количество различных ксенобиотиков как неорганической, так и органической природы, обладающих исключительной токсичностью.
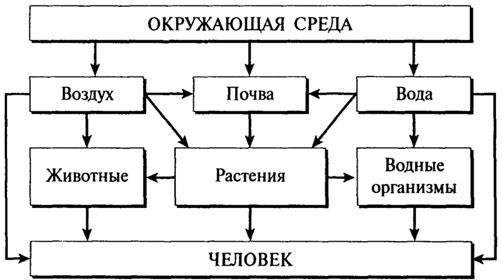
Рис. 2. Схема поступления ксенобиотиков из окружающей среды в организм человека по пищевым цепям
Антропогенная токсикация приобрела настолько значительные масштабы, что наносит ощутимый, реальный вред здоровью человека и грозит перерасти в экологическую катастрофу.
Вероятные чужеродные компоненты (ксенобиотики) представляют собой весьма широкий ассортимент веществ (около 3 тысяч) природного или антропогенного (сотворенного руками человека) происхождения, ненужных или даже вредных для организма человека, поступающих в организм с продуктами питания, но не являющихся питательными веществами, даже в небольших количествах обладающих негативной биологической активность, проявляющейся в токсическом, канцерогенном, аллергическом, мутагенном и тератогенном и других отрицательных действиях.
Последствия острого или хронического действия на организм ксенобиотиков, поступающих с пищей, называют пищевыми отравлениями. Они могут быть вызваны биоксенобиотиками (отравления микробного, грибкового, растительного и животного происхождения), химиоксенобиотиками (отравления пестицидами, солями тяжелых металлов, нитрозаминами, мигрантами из упаковки, посторонними механическими примесями минерального, металлического происхождения, сорными растениями и т.п.) и радиоксенобиотиками (поражения радиоактивными веществами – радионуклидами – естественного или антропогенного происхождения).
Ксенобиотики, попадая в окружающую среду в результате антропогенной деятельности человека, способны накапливаться в почвах, водоемах, с атмосферными и водными потоками распространяться на тысячи километров. Передвигаясь по пищевым цепям, ксенобиотики попадают в организм человека и вызывают серьезные нарушения здоровья — от острых отравлений с летальным исходом до заболеваний, проявляющихся порой только через годы (см. рис. 2).
2. Меры токсичности веществ. Количественная характеристика токсичности веществ достаточно сложна и требует многостороннего подхода. Судить о ней приходится по результатам воздействия вещества на живой организм, для которого характерна индивидуальная реакция, индивидуальная вариабельность, поскольку в группе испытуемых животных всегда присутствуют более или менее восприимчивые к действию изучаемого токсина индивидуумы.
Существуют две основные характеристики токсичности — ЛД50 и ЛД100. ЛД — аббревиатура летальной дозы, т. е. дозы, вызывающей при однократном введении гибель 50 или 100% экспериментальных животных. Дозу обычно определяют в размерности концентрации. Токсичными считают все те вещества, для которых ЛД мала. Принята следующая классификация веществ по признаку острой токсичности (ЛД50 для крысы при пероральном введении, мг/кг):
| Чрезвычайно токсичные | < 5 |
| Высокотоксичные | 5-50 |
| Умеренно токсичные | 50-500 |
| Малотоксичные | 500-5000 |
| Практически нетоксичные | 5000-15000 |
| Практически безвредные | > 15 000 |
Величина t0,5 характеризует время полувыведения токсина и продуктов его превращения из организма. Для разных токсинов оно может составлять от нескольких часов до нескольких десятков лет.
Кроме ЛД50, ДД100 и t0,5 в токсикологических экспериментах на животных принято указывать еще и время 100 или 50% гибели объектов. Но для этого такие эксперименты должны проводиться в течение многих месяцев и лет, а при существующем непродолжительном контроле можно отнести к малотоксичным веществам — высокотоксичные, но проявляющие свое негативное, губительное действие лишь через длительное время.
Антагонизм – эффект поздействия двух или нескольких веществ, при котором одно вещество ослабевает действие другого вещества (например, действие ртути и селена в организме животных и человека).
Синергизм – эффект воздействия, превышающий сумму эффектов воздействия каждого фактор (например, комбинированное воздействие хлоросодержащих соединений, фосфорорганических пестицидов, комбинированное воздействие ксенобиотиков и некоторых медикаментов).
В связи с хроническим воздействием посторонних веществ на организм человека и возникающей опасностью отдаленных последствий, важнейшее значение приобретают канцерогенное (возникновение раковых опухолей), мутагенное (качественные и количественные изменения в генетическом аппарате клетки) и тератогенное (аномалии в развитии плода, вызванные структурными, функциональными и биохимическими изменениями в организме матери и плода) действия ксенобиотиков.
На основе токсикологических критериев (с точки зрения гигиены питания) международными организациями ООН — ВОЗ, ФАО и др., а также органами здравоохранения отдельных государств приняты следующие базисные (основные) показатели: ПДК, ДСД и ДСП.
ПДК (предельно-допустимая концентрация) — предельно-допустимые количества чужеродных веществ в атмосфере, воде, продуктах питания о точки зрения безопасности их для здоровья человека. ПДК в продуктах питания — установленное законом предельно-допустимое с точки зрения здоровья человека количество вредного (чужеродного) вещества. ПДК — это такие концентрации, которые при ежедневном воздействии в течение сколь угодно длительного времени не могут вызывать заболеваний или отклонений в состоянии здоровья, обнаруживаемых современными методами исследований, в жизни настоящего и последующих поколений.
ДСД (допустимая суточная доза) — ежедневное поступление вещества, которое не оказывает негативного влияния на здоровье человека в течение всей жизни.
ДСП (допустимое суточное потребление) — величина, рассчитываемая как произведение ДСД на среднюю величину массы тела (60 кг).
3. Токсичные элементы. Токсичные элементы (в частности, некоторые тяжелые металлы) составляют обширную и весьма опасную в токсикологическом отношении группу веществ. Обычно рассматривают 14 элементов: Hg, Pb, Cd, As, Sb, Sn, Zn, Al, Be, Fe, Cu, Ba, Cr, Tl. Разумеется, не все перечисленные элементы являются ядовитыми, некоторые из них необходимы для нормальной жизнедеятельности, человека и животных. Поэтому часто трудно провести четкую границу между биологически необходимыми и вредными для здоровья человека веществами.
В большинстве случаев реализация того или иного эффекта зависит от концентрации. При повышении оптимальной физиологической концентрации элемента в организме может наступить интоксикация, а дефицит многих элементов в пище и воде может привести к достаточно тяжелым и трудно распознаваемым явлениям недостаточности.
4. Радиоактивное загрязнение. Источники радиоактивности, как и другие загрязнители, являются компонентами пищевых цепей: атмосфера—ветер— дождь—почва — растения – животные — человек. Анализируя данные о взаимодействии радионуклидов с компонентами природной среды и организмом человека, необходимо отметить следующее.
Радионуклиды естественного происхождения постоянно присутствуют во всех объектах неживой и живой природы, начиная с момента образования нашей планеты. При этом радиационный фон в различных регионах Земли может отличаться в 10 и более раз. К радионуклидам естественного происхождения относят, во- первых: космогенные радионуклиды, главным образом 3Н, 7Ве, 14С, 23Na, 24Na; во-вторых: радионуклиды, присутствующие в объектах окружающей среды (среди них основными источниками загрязнения пищевых продуктов и облучения человека являются 40К, 238U, 232Th).
Радон — один из первых открытых человеком радионуклидов. Этот благородный газ образуется при распаде изотопа 226Rа и поступает в организм ингаляционным путем. Человек контактирует с радоном везде, но главным образом в каменных и кирпичных жилых зданиях (особенно в подвальных помещениях и на первых этажах), поскольку главным источником является почва под зданием и строительные материалы.
Радиоактивность (мкЗв/год) строительных материалов такова:
- дерево 0;
- известняк, песчаник 0—100;
- кирпич, бетон 100—200;
- естественный камень, производственный гипс 200— 400;
- шлаковый камень, гранит 400—2000.
Высокое содержание радона может быть в подземных водах. Доступным и эффективным способом удаления радона из воды является ее аэрация.
В результате производственной деятельности человека, связанной с добычей полезных ископаемых, сжиганием органического топлива, созданием минеральных удобрений и т. п., произошло обогащение атмосферы естественными радионуклидами, причем естественный радиационный фон постоянно меняется.
С момента овладения человеком ядерной энергией в биосферу начали поступать радионуклиды, образующиеся на АЭС, при производстве ядерного топлива и испытаниях ядерного оружия. Таким образом, встал вопрос об искусственных радионуклидах и особенностях их влияния на организм человека. Среди радионуклидов искусственного происхождения выделяют 21 наиболее распространенный, 8 из которых составляют основную дозу внутреннего облучения населения: 14С, l37Cs, 90Sr, 89Sr, 106Ru, 144Ce, l311,95Zr.
Существуют три пути попадания радиоактивных веществ в организм человека:
- а) при вдыхании воздуха, загрязненного радиоактивными веществами;
- б) через желудочно-кишечный тракт — с пищей и водой;
- в) через кожу.
По характеру распределения в организме человека радиоактивные вещества можно условно разделить на следующие три группы.
- Отлагающиеся преимущественно в скелете (так называемые остеотропные изотопы — стронций, барий, радий и другие).
- Кoнцентрирующиеся в печени (церий, лантан, плутоний и другие).
- Равномерно распределяющиеся по системам (водород, углерод, инертные газы, железо и другие).
Причем одни имеют тенденцию к накоплению в мышцах (калий, рубидий, цезий), а другие — в селезенке, лимфатических узлах, надпочечниках (ниобий, рутений).
Особое место занимает радиоактивный иод — он селективно аккумулируется щитовидной железой.
3. Природные токсиканты
Природные токсины, не уступающие по канцерогенной активности антропогенным ксенобиотикам, из-за своей широкой распространенности и очень высокой степени нагрузки на организм человека представляют огромный риск для здоровья населения планеты. Это касается не только развивающихся стран, но и стран с развитой рыночной экономикой.
При остром воздействии наибольшую опасность представляют бактериальные токсины. С точки зрения хронического воздействия и опасности отдаленных последствий на первое место по степени риска выходят микотоксины.
Бактериальные токсины загрязняют пищевые продукты и являются причиной острых пищевых интоксикаций. Рассмотрим наиболее часто регистрируемые интоксикации, связанные с поражением пищевых продуктов некоторыми бактериальными токсинами.
Staphylococcus aureus — грамположительные бактерии, являются причиной стафилококкового пищевого отравления. Продуцируют семь энтеротоксинов: А, В, С,, С2, D, Е, которые представляют собой полипептиды с молекулярной массой 26 360—28 500 дальтон. Энтеротоксины S. aureus термостабильны и инактивируются лишь после 2—3 часового кипячения. Бактерицидным действием по отношению к стафилококкам обладают уксусная, лимонная, фосфорная, молочная кислоты при рН до 4,5. Кроме того, жизнедеятельность бактерий прекращается при концентрации соли (NaCl) — 12%, сахара — 60-70%, вакуумная упаковка также ингибирует рост бактерий. Все это необходимо учитывать в различных технологиях консервирования, как в промышленном масштабе, так и в домашних условиях.
Наиболее благоприятной средой для роста и развития стафилококков являются молоко, мясо и продукты их переработки, а также кондитерские кремовые изделия, в которых концентрация сахара составляет менее 50%. Стафилококковые энтеротоксины являются причиной 27— 45% всех пищевых токсикоинфекций.
Clostridium botulinum продуцирует токсины, представляющие особую опасность для человека. Эти микроорганизмы, являются облигатными анаэробами с термостабильными спорами. Различают А, В, С, D, E, F, G виды ботулотоксинов, причем наибольшей токсичностью обладают токсины А и Е. Ботулотоксины имеют белковую природу, молекулярная масса порядка 150 кДа.
Они поражают рыбные, мясные продукты, фруктовые, овощные и грибные консервы при недостаточной тепловой обработке и в условиях резкого снижения содержания кислорода (герметично закупоренные консервы). Кроме того, ботулотоксины характеризуются высокой устойчивостью к действию протеолитических ферментов, кислот, низких температур, но инактивируются под влиянием щелочей и высоких температур (80°С — 30 мин; 100°С — 15 мин).
Ботулизм встречается довольно часто (500—600 случаев в год), летальность достигает порядка 7—9%.
К токсинообразующим микроорганизмам, вызывающим пищевые отравления у человека, относятся также Clostridium perfringens — спорообразующие анаэробные грамположительные бактерии, которые продуцируют большое число энтеротоксинов.
Патогенные штаммы Escherichia coli являются продуцентами термостабильных токсинов полипептидной природы с молекулярной массой от 4 до 10 кДа и способны вызывать как острые токсиинфекции, так и являться причиной хронической интоксикации, в частности, являться причиной хронической почечной недостаточности.
Сырое молоко, мясо и мясные продукты, а также вода могут быть причиной возникновения заболеваний, связанных с присутствием патогенных штаммов Е. coli.
Микотоксины (от греч. mukes — гриб и toxicon — яд) — это вторичные метаболиты микроскопических плесневых грибов, обладающие выраженными токсическими свойствами. Они не являются эссенциальными для роста и развития продуцирующих их микроорганизмов.
В настоящее время из кормов и продуктов питания выделено около 250 видов плесневых грибов, большинство из которых продуцирует высокотоксичные метаболиты, в том числе около 120 микотоксинов. Предполагают, что с биологической точки зрения микотоксины выполняют в обмене веществ микроскопических грибов функции, направленные на выживание и конкурентоспособность в различных экологических нишах.
С гигиенических позиций — это особо опасные токсические вещества, загрязняющие корма и пищевые продукты. Высокая опасность микотоксинов выражается в том, что они обладают токсическим эффектом в чрезвычайно малых количествах и способны весьма интенсивно диффундировать в глубь продукта.
В настоящее время еще не сформирована единая классификация и номенклатура микотоксинов. В одних случаях в основу группового деления микотоксинов положена их химическая структура, в других — характер действия, в третьих — видовая принадлежность грибов-продуцентов.
Афлатоксины. Афлатоксины представляют собой одну из наиболее опасных групп микотоксинов, обладающих сильными канцерогенными свойствами.
Структура и продуценты афлатоксинов. В настоящее время семейство афлатоксинов включает четыре основных представителя (афлатоксины В1, В2, G1, G2) и еще более 10 соединений, являющихся производными или метаболитами основной группы (М1, М2, В2а, G2a, GM1, P1, Q1.
Физико-химические свойства афлатоксинов. Афлатоксины обладают способностью сильно флуоресцировать при воздействии длинноволнового ультрафиолетового излучения. Афлатоксины В1, и В2 обладают сине-голубой флуоресценцией, G1, и G2 — зеленой флуоресценцией, М1, и М2 — сине- фиолетовой. Это свойство лежит в основе практически всех физико- химических методов их обнаружения и количественного определения.
Афлатоксины слаборастворимы в воде (10—20 мкг/мл), нерастворимы в неполярных растворителях, но легко растворяются в растворителях средней полярности, таких как хлороформ, метанол и др. В химически чистом виде они относительно нестабильны и чувствительны к действию воздуха и света, особенно к ультрафиолетовому облучению. Растворы афлатоксинов стабильны в хлороформе и бензоле в течение нескольких лет при хранении в темноте и на холоде.
Следует обратить особое внимание на то, что афлатоксины практически не разрушаются в процессе обычной кулинарной и технологической обработки загрязненных пищевых продуктов.
Факторы, влияющие на токсинообразование. Продуценты афлатоксинов — микроскопические грибы рода Aspergillus могут достаточно хорошо развиваться и образовывать токсины на различных естественных субстратах (продовольственное сырье, пищевые продукты, корма), причем не только в странах с тропическим и субтропическим климатом, как полагали ранее, но практически повсеместно, за исключением, быть может, наиболее холодных районов Северной Европы и Канады.
Оптимальной температурой для образования токсинов является температура 27—30°С, хотя синтез афлатоксинов возможен и при более низкой (12—13°С) или при более высокой (40—42°С) температуре. Например, в условиях производственного хранения зерна максимальное образование афлатоксинов происходит при температуре 35—45°С, что значительно превышает температурный оптимум, установленный в лабораторных условиях.
Другим критическим фактором, определяющим рост микроскопических грибов и синтез афлатоксинов, является влажность субстрата и атмосферного воздуха. Максимальный синтез токсинов наблюдается обычно при влажности выше 18% для субстратов, богатых крахмалом (пшеница, ячмень, рожь, овес, рис, кукуруза, сорго), и выше 9—10% — для субстратов с высоким содержанием липидов (арахис, подсолнечник, семена хлопчатника, различные виды орехов). При относительной влажности атмосферного воздуха ниже 85% синтез афлатоксинов прекращается.
Биологическое действие афлатоксинов. Действие афлатоксинов на организм животных и человека может быть охарактеризовано с двух позиций. Во-первых, с точки зрения острого токсического действия и, во-вторых, сточки зрения оценки опасности отдаленных последствий. Острое токсическое действие афлатоксинов связано с тем, что они являются одними из наиболее сильных гепатропных ядов, органом-мишенью которых является печень. Отдаленные последствия действия афлатоксинов проявляются в виде канцерогенного, мутагенного и тератогенного эффектов.
Загрязнение пищевых продуктов афлатоксинами. Продуценты афлатоксинов встречаются повсеместно и этим объясняются значительные масштабы загрязнения кормов и пищевых продуктов и их существенная роль в создании реальной опасности для здоровья человека.
Частота обнаружения и уровень загрязнения афлатоксинами в значительной степени зависят от географических и сезонных факторов, а также от условий выращивания, уборки и хранения сельскохозяйственной продукции. В природных условиях чаще и в наибольших количествах афлатоксины обнаруживаются в арахисе, кукурузе, семенах хлопчатника. Кроме того, в значительных количествах они могут накапливаться в различных орехах, семенах масличных культур, пшенице, ячмене, зернах какао и кофе.
В кормах, предназначенных для сельскохозяйственных животных, афлатоксины также обнаруживаются достаточно часто и в значительных количествах. Во многих странах с этим связано и обнаружение афлатоксинов в продуктах животного происхождения. Например, в молоке и тканях сельскохозяйственных животных, получавших корма, загрязненные микотоксинами, обнаружен афлатоксин М1. Причем афлатоксин М1, обнаружен как в цельном молоке, так и в порошкообразном молоке, и даже в молочных продуктах, подвергшихся технологической обработке (пастеризация, стерилизация, приготовление творога, йогурта, сыров и т. п.).
Детоксикация загрязненных пищевых продуктов и кормов. Установление высокой токсичности и канцерогенности афлатоксинов и обнаружение их в значительных количествах в основных пищевых продуктах во всем мире привело к необходимости разработки эффективных методов детоксикации сырья, пищевых продуктов и кормов.
В настоящее время с этой целью применяют комплекс мероприятий, которые можно разделить на механические, физические и химические методы детоксикации афлатоксинов. Механические методы детоксикации связаны с отделением загрязненного сырья (материала) вручную или с помощью электронно-колориметрических сортировщиков.
Физические методы основаны на достаточно жесткой термической обработке материала (например, автоклавирование), а также связаны с ультрафиолетовым облучением и озонированием. Химический метод предполагает обработку материала сильными окислителями. К сожалению, каждый из названных методов имеет свои существенные недостатки: применение механических и физических методов не дает высокого эффекта, а химические методы приводят к разрушению не только афлатоксинов, но и полезных нутриентов и, кроме этого, нарушают их всасывание.
Согласно данным ВОЗ, человек при благоприятной гигиенической ситуации потребляет с суточным рационом до 0,19 мкг афлатоксинов. В России приняты следующие санитарно-гигиенические нормативы по афлатоксинам: ПДК афлатоксина В1 для всех пищевых продуктов, кроме молока, составляет — 5 мкг/кг, для молока и молочных продуктов — 1 мкг/кг (для афлатоксина М1 — 0,5 мкг/кг). Допустимая суточная доза (ДСД) — 0,005—0,01 мкг/кг массы тела.
Охратоксины. Охратоксины — соединения высокой токсичности, с ярко выраженным тератогенным эффектом. Продуцентами охратоксинов являются микроскопические грибы рода Aspergillus и Penicillium. Основными продуцентами являются A. ochraceus и P. viridicatum. Многочисленными исследованиями показано, что природным загрязнителем чаще всего является охратоксин А, в редких случаях охратоксин В.
Физико-химические свойства. Охратоксин А — бесцветное кристаллическое вещество, слабо растворимое в воде, умеренно растворимое в полярных органических растворителях (метанол, хлороформ), а также в водном растворе гидрокарбоната натрия. В химически чистом виде он нестабилен и очень чувствителен к воздействию света и воздуха, однако в растворе этанола может сохраняться без изменений в течение длительного времени. В ультрафиолетовом свете обладает зеленой флуоресценцией. Охратоксин В — кристаллическое вещество, аналог охратоксина А, не содержащий атом хлора. Он примерно в 50 раз менее токсичен, чем охратоксин А. В ультрафиолетом свете обладает голубой флуоресценцией. Охратоксин С — аморфное вещество, этиловый
Методы определения микотоксинов. Современные методы обнаружения и определения содержания микотоксинов в пищевых продуктах и кормах включают скрининг- методы, количественные аналитические и биологические методы.
Скрининг-методы отличаются быстротой и удобны для проведения серийных анализов, позволяют быстро и надежно разделять загрязненные и незагрязненные образцы. К ним относятся такие широко распространенные методы, как миниколоночный метод определения афлатоксинов, охратоксина А и зеараленона; методы тонкослойной хроматографии (ТСХ-методы) для одновременного определения до 30 различных микотоксинов, флуоресцентный метод определения зерна, загрязненного афлатоксинами, и некоторые другие.
Количественные аналитические методы определения микотоксинов представлены химическими, радиоиммунологическими и иммуноферментными методами. Химические методы являются в настоящее время наиболее распространенными и состоят из двух стадий: стадии выделения и стадии количественного определения микотоксинов. Стадия выделения включает экстракцию (отделение микотоксина от субстрата) и очистку (отделение микотоксина от соединений с близкими физико-химическими характеристиками).
Окончательное разделение микотоксинов проводится с помощью различных хроматографических методов, таких как газовая (ГХ) и газожидкостная хроматография (УЖУ), тонкослойная хроматография (ТСХ), высокоэффективная жидкостная хроматография (ВЭЖХ) и масс- спектрометрия. Количественную оценку содержания микотоксинов проводят путем сравнения интенсивности флуоресценции при ТСХ в ультрафиолетовой области спектра со стандартами. Для подтверждения достоверности полученных результатов применяют различные тесты, основанные на получении производных микотоксинов с иными хроматографическими, колориметрическими или флюорометрическими характеристиками.
Высокочувствительные и высокоспецифичные радиоиммуно-химические и иммуноферментные методы обнаружения, идентификации и количественного определения микотоксинов находят все более широкое применение и пользуются повышенным вниманием со стороны исследователей. Эти методы основаны на получении антисывороток к конъюгатам микотоксинов с бычьим сывороточным альбумином. Основным преимуществом этих методов является их исключительная чувствительность.
Биологические методы обычно не отличаются высокой специфичностью и чувствительностью и применяются, главным образом, в тех случаях, когда отсутствуют химические методы выявления микотоксинов или в дополнение к ним в качестве подтверждающих тестов. В качестве тест — объектов используют различные микроорганизмы, куриные эмбрионы, различные лабораторные животные, культуры клеток и тканей.
Контроль за загрязнением микотоксинами. В настоящее время вопросы контроля за загрязнением продовольственного сырья, пищевых продуктов и кормов микотоксинами решаются не только в рамках отдельных государств, но и на международном уровне, под эгидой ВОЗ и ФАО.
В системе организации контроля за загрязнением продовольственного сырья и пищевых продуктов можно выделить два уровня: инспектирование и мониторинг, которые включают регулярные количественные анализы продовольственного сырья и пищевых продуктов.
Мониторинг позволяет установить уровень загрязнения, оценить степень реальной нагрузки и опасности, выявить пищевые продукты, являющиеся наиболее благоприятным субстратом для микроскопических грибов — продуцентов микотоксинов, а также подтвердить эффективность проводимых мероприятий по снижению загрязнения микотоксинами. Особое значение имеет контроль за загрязнением микотоксинами при характеристике качества сырья и продуктов, импортируемых из других стран.
С целью профилактики алиментарных токсикозов основное внимание следует уделять зерновым культурам. В связи с этим необходимо соблюдать следующие меры по предупреждению загрязнения зерновых культур и зерно продуктов.
- Своевременная уборка урожая с полей, его правильная агротехническая обработка и хранение.
- Санитарно-гигиеническая обработка помещений и емкостей для хранения.
- Закладка на хранение только кондиционного сырья.
- Определение степени загрязнения сырья и готовых продуктов.
- Выбор способа технологической обработки в зависимости от вида и степени загрязнения сырья.
4. Антиалиментарные факторы питания
Помимо чужеродных соединений, загрязняющих пищевые продукты, так называемых контаминантов -загрязнителей, и природных токсикантов, необходимо учитывать действие веществ, не обладающих общей токсичностью, но способных избирательно ухудшать или блокировать усвоение нутриентов. Эти соединения принято называть антиалиментарными факторами питания. Этот термин распространяется только на вещества природного происхождения, которые являются составными частями натуральных продуктов питания.
Перечень антиалиментарных факторов питания достаточно обширен.
Остановимся на рассмотрении:
Ингибиторы пищеварительных ферментов. К этой группе относятся вещества белковой природы, блокирующие активность пищеварительных ферментов (пепсин, трипсин, химотрипсин, α-амилаза). Белковые ингибиторы обнаружены в семенах бобовых культур (соя, фасоль и др.), злаковых (пшеница, ячмень и др.), в картофеле, яичном белке и других продуктах растительного и животного происхождения.
Механизм действия этих соединений заключается в образовании стойких комплексов «фермент-ингибитор», подавлении активности главных пищеварительных ферментов и, тем самым, снижении усвоения белковых веществ и других макронутриентов.
К настоящему времени белковые ингибиторы достаточно хорошо изучены и подробно охарактеризованы: расшифрована первичная структура, изучено строение активных центров ингибиторов, исследован механизм действия ингибиторов и т. п.
На основании структурного сходства все белки-ингибиторы растительного происхождения можно разделить на несколько групп, основными из которых являются следующие.
- Семейство соевого ингибитора трипсина (ингибитора Кунитца).
- Семейство соевого ингибитора Баумана—Бирка.
- Семейство картофельного ингибитора I.
- Семейство картофельного ингибитора П.
- Семейство ингибиторов трипсина / α-амилазы.
Ингибитор Кунитца был впервые выделен из семян сои еще в 1946 г. Его молекулярная масса 20 100 Да. Молекула ингибитора состоит из 181 аминокислотного остатка и содержит две дисульфидные связи в положении цис(39) — цис(86) и цис(136) — цис(145). Трипсиносвязывающий реактивный центр включает остаток аргинина, связанный пептидной связью с остатком изолейцина: арг(63) — иле(64), поэтому ингибиторы этого семейства также называют трипсиновыми ингибиторами аргининового типа.
Ингибитор Баумана—Бирка был впервые выделен также в 1946 г. из семян сои. Ингибитор эффективно подавляет активность трипсина и химотрипсина, причем с одной молекулой ингибитора могут связываться молекулы обоих ферментов. Ингибитор Баумана—Бирка — первый описанный «двуглавый» (или двухцентровой) ингибитор сериновых протеиназ. Его молекулярная масса примерно 8000 Да. Молекула ингибитора состоит из 71 аминокислотного остатка. Особенностью аминокислотного состава является высокое содержание остатков цистеина (7 на одну молекулу) и отсутствие остатков глицина и триптофана.
Обращает на себя внимание, что молекула ингибитора Баумана—Бирка состоит из двух частей, сходных по структуре (доменов), которые соединены между собой короткими полипептидными цепочками. Реактивный центр, ответственный за связывание трипсина, локализован в первом домене и содержит пептидную связь: лиз(16) — сер(17); а реактивный центр, ответственный за связывание химотрипсина, находится во втором домене и содержит пептидную связь: лей(43) — сер(44), поэтому ингибиторы этого семейства иногда называют ингибиторами ли-зиновоготипа.
В клубнях картофеля содержится целый набор ингибиторов химотрипсина и трипсина, которые отличаются по своим физико-химическим свойствам: молекулярной массе, особенностям аминокислотного состава, изоэлектрическим точкам, термо- и рН-стабильности и т. п. Кроме картофеля, белковые ингибиторы обнаружены в других пасленовых, а именно — в томатах, баклажанах, табаке. Наряду с ингибиторами сериновых протеиназ в них обнаружены и белковые ингибиторы цистеиновых, аспартильных протеиназ, а также металлоэкзопептидаз.
Заслуживает внимания и тот факт, что в семенах растений и в клубнях картофеля находятся «двуглавые» ингибиторы, способные одновременно связываться и ингибировать протеазу и α-амилазу. Такие белковые ингибиторы были выделены из риса, ячменя, пшеницы, тритикале, ржи.
Рассматриваемые белковые ингибиторы растительного происхождения характеризуются высокой термостабильностью, что в целом не характерно для веществ белковой природы. Например, полное разрушение соевого ингибитора трипсина достигается лишь 20 минутным автоклавированием при 115°С, или кипячением соевых бобов в течение 2—3 часов. Из этого следует, что употребление семян бобовых культур, особенно богатых белковыми ингибиторами пищеварительных ферментов, как для корма сельскохозяйственных животных, так и в пищевом рационе человека, возможно лишь после соответствующей тепловой обработки.
Цианогенные гликозиды. Цианогенные гликозиды — это гликозиды некоторых цианогенных альдегидов и кетонов, которые при ферментативном или кислотном гидролизе выделяют синильную кислоту — HCN, вызывающую поражение нервной системы.
Из представителей цианогенных гликозидов целесообразно отметить лимарин, содержащийся в белой фасоли, и амигдалин, который обнаруживается в косточках миндаля (до 8%), персиков, слив, абрикос (от 4 до 6%).
Амигдалин представляет собой сочетание дисахарида гентиобиозы и агликона, включающего остаток синильной кислоты и бензальдегида.
Биогенные амины. К соединениям этой группы относятся серотонин, тирамин, гистамин — биогенные амины, обладающие сосудосуживающим действием.
Серотонин, главным образом, содержится во фруктах и овощах. Например, содержание серотонина в томатах — 12 мг/кг; в сливе — до 10 мг/кг. Тирамин чаще всего обнаруживается в ферментированных продуктах, например в сыре до 1100 мг/кг. Содержание гистамина коррелирует с содержанием тирамина в сыре от 10 до 2500 мг/кг. В количествах более 100 мг/кг гистамин может представлять угрозу для здоровья человека.
Алкалоиды, Алкалоиды — весьма обширный класс органических соединений, оказывающих самое различное действие на организм человека. Это и сильнейшие яды, и полезные лекарственные средства. Печально известный наркотик, сильнейший галлюциноген — ЛСД — диэтиламидлизергиловой кислоты, был выделен из спорыньи, грибка, растущего на ржи, в 1943 г. швейцарским химиком А. Гофманом.
С 1806 г. известен морфин, он выделен из сока головок мака и является очень хорошим обезболивающим средством, благодаря чему нашел применение в медицине, однако при длительном употреблении приводит к развитию наркомании.
Содержание кофеина в сырье и различных продуктах колеблется в достаточно широких пределах. В зернах кофе и листьях чая, в зависимости от вида сырья, от 1 до 4%; в напитках кофе и чая, в зависимости от способа приготовления, до 1500 мг/л (кофе) и до 350 мг/л (чай). В напитках пепси-кола и кока-кола до 1000 мг/л и выше. Здесь уместно подчеркнуть, что пуриновые алкалоиды при систематическом употреблении их на уровне 1000 мг в день вызывают у человека постоянную потребность в них, напоминающую алкогольную зависимость.
К группе стероидных алкалоидов будут относится соланины и чаконины, содержащиеся в картофеле. Иначе их называют гликоалкалоидами, они содержат один и тот же агликон (соланидин), но различные остатки сахаров. В картофеле обнаружены шесть гликоалкалоидов, одним из которых является α- соланин.
Таким образом, гликоалкалоиды картофеля весьма близки по составу и являются промежуточными продуктами при биосинтезе α-соланина. Это вещества средней токсичности, их накопление в клубнях картофеля (в позеленевших частях клубня их количество может увеличиваться более чем в 10 раз и достигать 500 мг/кг), придает горький вкус и вызывает типичные признаки отравления. Эти соединения обладают антихолин-эстеразной активностью.
Соланины и чаконины могут содержаться в баклажанах, томатах, табаке.
Антивитамины. Согласно современным представлениям, к антивитаминам относят две группы соединений.
- я группа — соединения, являющиеся химическими аналогами витаминов, с замещением какой-либо функционально важной группы на неактивный радикал, т. е. это частный случай классических антиметаболитов.
- я группа — соединения, тем или иным образом специфически инактивирующие витамины, например с помощью их модификации, или ограничивающие их биологическую активность.
Если классифицировать антивитамины по характеру действия, как это принято в биохимии, то первая (антиметаболитная) группа может рассматриваться в качестве конкурентных ингибиторов, а вторая — неконкурентных, причем во вторую группу попадают весьма разнообразные по своей химической природе соединения и даже сами витамины, способные в ряде случаев ограничивать действие друг друга.
Рассмотрим некоторые конкретные примеры соединений, имеющих ярко выраженную антивитаминную активность.
Лейцин — нарушает обмен триптофана, в результате чего блокируется образование из триптофана ниацина — одного из важнейших водорастворимых витаминов — витамина PP.
Индолилуксусная кислота и ацетилпиридин — также являются антивитаминами по отношению к витамину РР; содержатся в кукурузе.
Чрезмерное употребление продуктов, содержащих вышеуказанные соединения, может усиливать развитие пеллагры, обусловленной дефицитом витамина PP.
Аскорбатоксидаза и некоторые другие окислительные ферменты проявляют антивитаминную активность по отношению к витамину С. Аскобатоксидаза (Н. Ф. 1.10.3.3) катализирует реакцию окисления аскорбиновой кислоты в дегидроаскорбиновую кислоту.
Содержание аскорбатоксидазы и ее активность в различных продуктах неодинакова: наиболее активна аскорбатоксидаза в огурцах, кабачках, наименее — в моркови, свекле, помидорах. При измельчении овощей за 6 часов хранения теряется более половины витамина С, т. к. измельчение способствует взаимодействию фермента и субстрата.
Тиаминаза (Н. Ф. 3.5.99.2) — антивитаминный фактор для витамина В1 — тиамина. Она содержится в продуктах растительного и животного происхождения, наибольшее содержание этого фермента отмечено у пресноводных и морских рыб, кроме того, тиаминаза продуцируется бактериями кишечного тракта — Вас. thiaminolytic и Вас. anekrinolytieny, что может являться причиной дефицита тиамина. Ортодифенолы и биофлавоноиды (вещества с Р-витаминной активностью), содержащиеся в кофе и чае, а также окситиамин, который образуется при длительном кипячении кислых ягод и фруктов, проявляют антивитаминную активность по отношению к тиамину.
Все это необходимо учитывать при употреблении, приготовлении и хранении пищевых продуктов.
Линатин — антагонист витамина В6, содержится в семенах льна. Кроме этого, ингибиторы пиродоксалевых ферментов обнаружены в съедобных грибах и некоторых видах семян бобовых.
Авидин — белковая фракция, содержащаяся в яичном белке, приводящая к дефициту биотина (витамина Н), за счет связывания и перевода его в неактивное состояние.
Гидрогенизированные жиры — являются факторами, снижающими сохранность витамина А — ретинола.
Говоря об антиалиментарных факторах питания, нельзя не сказать о гипервитаминозах. Известны два типа: гипервитаминоз А и гипервитаминоз D. Например, печень северных морских животных несъедобна из-за большого содержания витамина А.
Факторы, снижающие усвоение минеральных веществ. К. факторам, снижающим усвоение минеральных веществ, в первую очередь следует отнести щавелевую кислоту и ее соли (оксалаты), фитин (инозитолгексафосфорная кислота) и танины.
Наиболее изучена в этом плане щавелевая кислота. Продукты с высоким содержанием щавелевой кислоты способны приводить к серьезным нарушениям солевого обмена, необратимо связывать ионы кальция. Установлено, что интоксикация щавелевой кислотой проявляется в большей степени на фоне дефицита витамина D.
Известны случаи отравлений с летальным исходом, как от самой щавелевой кислоты (при фальсификации продуктов, в частности вин, когда подкисление проводили дешевой щавелевой кислотой), так и от избыточного потребления продуктов, содержащих ее в больших количествах. Смертельная доза для взрослых людей колеблется от 5 до 150 г и зависит от целого ряда факторов. Содержание щавелевой кислоты в среднем в некоторых растениях таково (в мг/100г): шпинат—1000, ревень — 800, щавель — 500, красная свекла — 250.
Фитин, благодаря своему химическому строению, легко образует труднорастворимые комплексы с ионами Са, Mg, Fe, Zn, и Сu. Этим объясняется его деминерализующий эффект.
Достаточно большое количество фитина содержится в злаковых и бобовых культурах: в пшенице, горохе, кукурузе его содержание примерно 400 мг/100 г продукта, причем основная часть сосредоточена в наружном слое зерна. Хлеб, выпеченный из муки высшего сорта, практически не содержит фитина. В хлебе из ржаной муки его мало, благодаря высокой активности фитазы, способной расщеплять фитин.
Дубильные вещества, кофеин, балластные соединения могут рассматриваться как факторы, снижающие усвоение минеральных веществ.
Яды пептидной природы. Многие биологически активные вещества являются циклопептидами, т. е. имеют циклическое строение. К таким циклопептидам относятся антибиотики, гормоны и токсины. Было показано, что ядовитый гриб бледная поганка (Amanita phalloides) содержит не менее десяти токсичных циклопептидов. Их молекулярная масса около 1000; они содержат атом серы, принадлежащий к остатку цистеина, связанному с индольным кольцом триптофана.
Алкоголь. Алкоголь можно рассматривать как рафинированный продукт питания, который имеет только энергетическую ценность. При окислении 1 г этанола выделяется 7 ккал энергии; данная величина лежит между калорийностью углеводов и жиров. Алкоголь не является источником каких- либо пищевых веществ, поэтому его часто называют источником «холостых» калорий.
Попадая в организм человека, этанол под воздействием фермента — алкогольдегидрогеназы окисляется до ацетальдегида, далее ацетоалъдегид под воздействием другого фермента — альдегиддегидрогеназы окисляется до ацетата. В результате этих двух реакций образуются две молекулы НАДН, которые служат донорами водорода в дыхательной цепи митохондрий. В ходе последующего переноса электронов к кислороду из ДДФ и остатка фосфорной кислоты образуется 6 молекул АТФ. Образовавшийся из этанола ацетат в дальнейшем активируется и переходит в ацетил-кофермент А. Образовавшийся ацетил-КоА, в свою очередь, может окисляться в цикле лимонной кислоты.
Алкоголь синтезируется ферментными системами организма для собственных нужд и в течение дня организм человека способен синтезировать от 1 до 9 г этилового спирта. Эндогенный алкоголь является естественным метаболитом, и ферментных мощностей организма вполне хватает для его окисления в энергетических целях. При потреблении алкоголя в больших количествах ферменты не справляются, происходит накопление этилового спирта и уксусного альдегида, что вызывает симптомы обширной интоксикации (головная боль, тошнота, аритмия сердечных сокращений). Таким образом, алкоголь можно рассматривать как антиалиментарный фактор питания, приводящий к специфическим нарушениям обмена веществ.
У людей, потребляющих большие количества алкоголя, обнаруживается дефицит незаменимых веществ. Примером могут служить тяжелые формы недостаточности витаминов у алкоголиков: алкогольные формы полиневрита, пеллагры, бери-бери и т. п., а также гипогликемия, т. к. этанол блокирует синтез глюкозы из лактата и аминокислот.
Хроническое потребление алкогольных напитков приводит не только к авитаминозам, но и к нарушению углеводного, жирового и белкового обмена и заканчивается, как правило, биохимической катастрофой с тяжелыми патологиями. Кроме того, совершенно очевидно, что алкоголь обладает наркотическим действием, вызывая устойчивую зависимость, которая приводит к негативным изменениям психики и, в конечном счете, к деградации личности.
5. Метаболизм чужеродных соединений
Механизм детоксикации ксенобиотиков — две фазы. Изучение метаболизма чужеродных соединений, превращений, которые они претерпевают, попадая в организм человека, важны, в первую очередь, с точки зрения выяснения химических и биохимических механизмов детоксикации, а также с точки зрения оценки возможностей защитной системы организма по детоксикации чужеродных веществ.
Метаболизм чужеродных соединений в организме будет зависеть от множества различных факторов. Путь ксенобиотика, его воздействие и ответную реакцию организма можно представить в виде схемы (см. рис. 4).
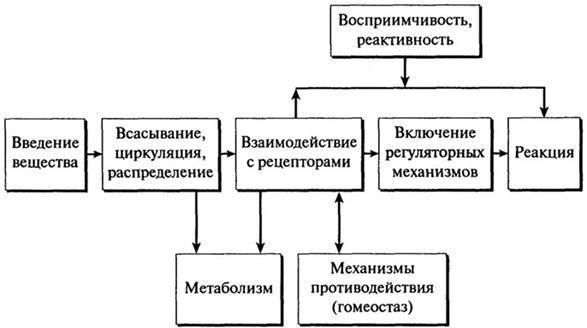
Рис. 4. Путь и воздействие ксенобиотика в организм человека
Попадая в организм, определенная доза вещества всасывается в месте контакта, разносится и распределяется в крови и органах. Вследствие метаболистических изменений и ритмического протекания процессов детоксикации уровень его содержания падает. В тканях и клетках ксенобиотик проходит через одну или несколько мембран, взаимодействуя с рецепторами. В результате возникает ответная реакция, включаются механизмы противодействия с целью поддержания постоянства внутренней среды — гомеостаза.
Метаболизм ксенобиотиков протекает в виде двухфазного процесса:
- 1-я фаза — метаболистические превращения;
- 2-я фаза — реакции конъюгации.
- 3-я фаза (метаболистические превращения) —связана с реакциями окисления, восстановления, гидролиза и протекает при участии ферментов, главным образом, в эндоплазматическом ретикулуме печени и реже — других органов (надпочечниках, почках, кишечнике, легких и т. д.).
- 4-я фаза (реакции конъюгации) — это реакции, приводящие к детоксикации.
Наиболее важные из них — это реакции связывания активных — ОН, —NH2, —СООН и —SH-групп и метаболита первичного ксенобиотика. Интересно, что некоторые ксенобиотики, в частности лекарственные средства, могут стимулировать активность ферментов, участвующих в метаболизме различных веществ (не только собственном). Такая ферментативная индукция может считаться выгодной, т. к. метаболизм и выведение токсических веществ ускоряется, если только промежуточные метаболиты не окажутся более токсичными, чем исходные вещества.
Факторы, влияющие на метаболизм чужеродных соединений. Чужеродные соединения обычно метаболизируются различными путями, образуя множество метаболитов. Скорость и направление этих реакций зависят от многих факторов, результатом действия которых могут быть изменения в картине метаболизма и, как следствие, возникают различия в токсичности. Эти факторы по своему происхождению можно разделить на:
- а) генетические (генетически обусловленные дефекты ферментов, участвующие в метаболизме чужеродных соединений);
- б) физиологические (возраст, пол, состояние питания, наличие различных заболеваний);
- в) факторы окружающей среды (облучение ионизирующей радиацией, стресс из-за неблагоприятных условий, наличие других ксенобиотиков).
Очень важно для процессов детоксикации, чтобы обе фазы детоксикации функционировали согласованно.
6. Фальсификация пищевых продуктов
С точки зрения безопасности продуктов питания значительную опасность могут представлять и некоторые виды фальсификации пищевых продуктов. Как правило, это виды ассортиментной фальсификации, которые могут привести к использованию опасных заменителей. Виды таких фальсификаций разнообразны. Примерами могут служить:
- фальсификация алкогольных напитков путем частичной или полной замены пищевого этилового спирта техническим спиртом, содержащим вредные примеси;
- приготовление «искусственных» вин; использование запрещенных пищевых добавок или применение их в повышенных количествах;
- недостаточное отделение примесей в крупяных продуктах;
- использование загрязненного растительного сырья, больных животных, испорченных полуфабрикатов и т. д.
В каждом конкретном случае требуется специальная гигиеническая оценка, основанная на современной нормативно-методической базе и осуществляемая государственными органами надзора за качеством и безопасностью пищевых продуктов.
Особый интерес представляют так называемые генетически модифицированные (трансгенные) продукты питания. Сообщения о генетически модифицированных растениях и полученных из них продуктах питания появились в начале 90-х гг. В настоящее время генетическому изменению подвергается важнейшее растительное сырье, а ведь без использования растительного сырья получают лишь очень немногие продукты.
Успехи в области генной инженерии позволяют получать новые сорта растений (причем в течение всего 2—3 лет) с заданными свойствами. За счет встраивания генов, выделенных из одних организмов и несущих определенную генетическую информацию (например, устойчивость к заморозкам, гербицидам, болезням и паразитам, высокая урожайность, неполегаемость и др.) в ДНК других, были получены растения, которые называют трансгенными, т. е. с перемещенными генами.
В США в настоящее время насчитывается более 100 наименований генетически измененных продуктов, а площади в разных странах, на которых произрастают трансгенные растения, составляют по разным оценкам от 10 до 25 млн гектар. Трансгенные растения выращивают в США, Канаде, Японии, Китае, Бразилии, Аргентине и многих других странах. Европейские государства занимают в этом отношении более жесткую позицию.
К трансгенным продуктам можно отнести генетически измененную сою, устойчивую к гербицидам. Как известно, соя используется для приготовления 30 000 пищевых продуктов: супов, детского питания, картофельных чипсов, маргарина, салатных соусов, рыбных консервов и др. Кроме сои, наибольшее распространение получили трансгенные помидоры, кукуруза, рис, картофель, клубника, а также генетически модифицированные дрожжи и ферментные препараты, полученные из трансгенных микроорганизмов. Генная инженерия находит применение и в животноводстве, влияя на рост и продуктивность сельскохозяйственных животных.
Безопасность генетически модифицированных продуктов питания остается все еще под вопросом. Нет и не может быть однозначного ответа на вопрос о возможной опасности отдаленных последствий таких продуктов. Очевидно одно — трансгенная продукция должна проходить тщательную многофакторную проверку на безопасность и иметь специальную маркировку. Однако и в этом пока больше вопросов, чем ответов.
Все большее число стран старается регламентировать продажу «новых» пищевых продуктов. Так в законе, принятом Евро парламентом, на упаковках нерафинированного масла и попкорна из генетически измененной кукурузы должна быть соответствующая маркировка, а на упаковке с крахмалом или полученным из него глюкозным сиропом подобной маркировки не требуется. Маркировка не требуется и на упаковке с рафинированным маслом или изготовленным из него майонезом.
Полученные из генетически измененного яблока мусс или яблочный сок должны нести соответствующую маркировку, а яблочный уксус — нет. Не фиксируется факт использования генетически измененного сырья при изготовлении лецитина и получении с его помощью шоколада и крема. Должны иметь соответствующую маркировку соевый шрот, белок, полученный из него, и готовые супы с данным белком. Корма для животных, полученные из шрота генетически измененной сои, не маркируются.
Таким образом, в странах Евросоюза в настоящее время барьер перед генетически измененной пищей сломан, однако к потребителю допускается пища, в которой обнаруживаются только следы генетических изменений.
В России с 1 июля 1999 г. вступило в силу постановление Министерства здравоохранения РФ «О порядке гигиенической оценки и регистрации пищевой продукции, полученной из генетически модифицированных источников».
Согласно этому документу гигиеническая экспертиза пищевых продуктов и продовольственного сырья, а также компонентов (фрагментов) для их производства, полученных из генетически модифицированных источников, должна включать определение вносимой последовательности генов, маркерных генов антибиотиков, промотеров, стабильности генетически модифицированных организмов на протяжении нескольких поколений, а также санитарно-химические показатели качества и безопасности, результаты токсикологических исследований на лабораторных животных, оценку аллергенных свойств продукта, возможных мутагенных, канцерогенных и тератогенных эффектов.
Кроме этого, обязательна технологическая оценка пищевой продукции, полученной из генетически модифицированного сырья — органолептических свойств и физико-химических параметров.
Заключение
Приведенные выше данные свидетельствуют о необходимости дальнейшего тщательного изучения вопросов, связанных с взаимодействием различных природных компонентов пищевого сырья и продуктов питания, влияния на них различных способов технологической и кулинарной обработки, а также режимов и сроков хранения с целью снижения потерь ценных макро- и микронутриентов, и обеспечения рациональности и адекватности питания.


