Содержание страницы
Пищевые кислоты представляют собой разнообразную по своим свойствам группу веществ органической и неорганической природы.
Состав и особенности химического строения пищевых кислот различны и зависят от специфики пищевого объекта, а также природы кислотообразования.
В большинстве растительных объектов обнаружены нелетучие моно- и трикарбоновые кислоты, предельные и непредельные, в том числе гидрокси- и оксокислоты.
В продуктах переработки плодов, например в мезге, могут быть выявлены летучие кислоты — муравьиная и уксусная.
Кислотность молока и молочных продуктов формируется как за счет молочной кислоты, образуемой в результате биохимических превращений лактозы молока, так и за счет других, содержащихся в молоке кислот и кислых солей, а также кислотных групп казеина.
Названия и формулы некоторых кислот, наиболее часто встречающихся в пищевых продуктах, представлены в табл. 1.
Таблица 1. Названия и формулы основных пищевых кислот
| Название кислоты | Название ионизированной формы кислоты | Формула |
| Аскорбиновая | Аскорбат | 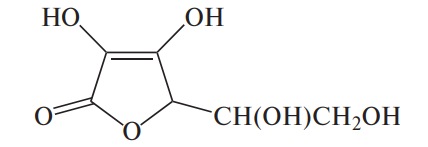 |
| Аспарагиновая | Аспартат | HООC–СН2–СН(NН2)–СООН |
| Бензойная | Бензоат | С6Н5–СООН |
| Винная | Тартрат | HООC–СН(ОН)–СН(ОН)–СООН |
| Гликолевая | Гликолат | HОСН2–СООН |
| Глицериновая | Глицерат | HОСН2–СН(ОН)–СООН |
| Глутаминовая | Глутамат | HООC–(СН2)2–СН(NН2)–СООН |
| Изолимонная | Изоцитрат | HООC–СН(ОН)–СН(СООН)–СН2–СООН |
| -Kетоглутаровая | Kетоглутарат | HООC–С(О)–(СН2)2–СООН |
| Лимонная | Цитрат | (HOOC–СН2)2–С(ОН)–СООН |
| Молочная | Лактат | СН3–СН(ОН)–СООН |
| Муравьиная | Формиат | НСООН |
| Пировиноградная | Пируват | СН3–С(О)–СООН |
| Пироглутаминовая | Пироглутамат | 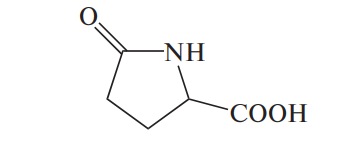 |
| Соляная | Хлорид | НСl |
| Серная | Сульфат | Н2SО4 |
| Уксусная | Ацетат | СН3–СООН |
| Фосфорная | Фосфат | Н3РО4 |
| Фумаровая | Фумарат | транс-СООН–СН=СН–СООН |
| Хинная | Хиннат | 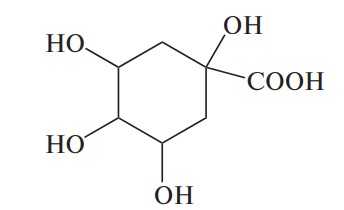 |
| Шикимовая | Шикимат | 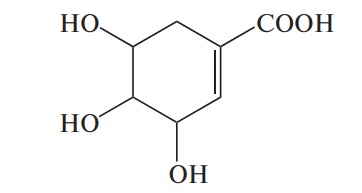 |
| Щавелевая | Оксалат | HООC–СООН |
| Щавелевоуксусная | Оксалоацетат | HООC–С(О)–СН2–СООН |
| Яблочная | Малат | HООC–СН2–СН(ОН)–СООН |
| Янтарная | Сукцинат | HООC–СН2–СН2–СООН |
К группе органических пищевых кислот в принципе относятся также аминокислоты, входящие в состав белков, и высшие жирные кислоты, являющиеся структурными компонентами липидов. Свойства и значение этих групп кислот рассматриваются в п. 3 и 1.
1. Общая характеристика кислот пищевых объектов
Основные источники пищевых кислот — растительное сырье и продукты его переработки. Органические пищевые кислоты содержатся в большинстве видов растительных пищевых объектов — ягодах, фруктах, овощах, в том числе в корнеплодах, лиственной зелени. Наряду с сахарами и ароматическими соединениями они формируют вкус и аромат плодов и, следовательно, продуктов их переработки.
Общее представление о разнообразии пищевых кислот в составе растительных объектов иллюстрирует табл. 2.
Таблица 2. Некоторые пищевые кислоты фруктов, ягод и овощей
| Растительный объект | Основные кислоты | |
| Фрукты, ягоды | ||
| Абрикосы | Яблочная, лимонная | |
| Авокадо | Винная | |
| Айва | Яблочная (без лимонной) | |
| Ананасы | Лимонная, яблочная | |
| Апельсины | Лимонная, яблочная, щавелевая | |
| Апельсиновая кожура (цедра) | Яблочная, лимонная, щавелевая | |
| Бананы | Яблочная, лимонная, винная, следы уксусной и муравьиной | |
| Виноград | Яблочная и винная (3:2), лимонная, щавелевая | |
| Вишня | Яблочная, лимонная, винная, янтарная, хинная, шикимовая, глицериновая, гликолевая | |
| Грейпфрут | Лимонная, винная, яблочная, щавелевая | |
| Груши | Яблочная, лимонная, винная, щавелевая | |
| Ежевика | Изолимонная, яблочная, молочно-изолимонная, шикимовая, хинная, следы лимонной и щавелевой | |
| Клубника | Лимонная, яблочная, шикимовая, янтарная, глицериновая, | |
| (земляника) | гликолевая, аспарагиновая | |
| Клюква | Лимонная, яблочная, бензойная | |
| Крыжовник | Лимонная, яблочная, шикимовая, хинная | |
| Лаймы | Лимонная, яблочная, винная, щавелевая | |
| Лимоны | Лимонная, яблочная, винная, щавелевая (без изолимонной) | |
| Персики | Яблочная, лимонная | |
| Сливы | Яблочная, винная, щавелевая | |
| Смородина | Лимонная, винная, яблочная, янтарная | |
| Финики | Лимонная, яблочная, уксусная | |
| Черника | Лимонная, яблочная, глицериновая, лимонно-яблочная, гликолевая, янтарная, глюкуроновая, галактуроновая, хинная, глутаминовая, аспарагиновая | |
| Яблоки | Яблочная, хинная, а-кетоглутаровая, щавелевоуксусная, лимонная, пировиноградная, фумаровая, молочная, янтарная | |
|
Овощи |
||
| Бобы | Лимонная, яблочная, небольшие количества янтарной и фумаровой | |
| Брокколи | Яблочная и лимонная (3 : 2), щавелевая, янтарная | |
| Грибы | Кетостеариновая, фумаровая, аллантоиновая | |
| Горох | Яблочная | |
| Картофель | Яблочная, лимонная, щавелевая, фосфорная, пироглутаминовая | |
| Морковь | Яблочная, лимонная, изолимонная, янтарная, фумаровая | |
| Помидоры | Лимонная, яблочная, щавелевая, янтарная, гликолевая, винная, фосфорная, соляная, серная, фумаровая, галактуроновая | |
| Ревень | Яблочная, лимонная, щавелевая | |
Наиболее типичными в составе различных плодов и ягод являются лимонная и яблочная кислоты. Из числа других кислот часто обнаруживаются хинная, янтарная и щавелевая. К распространенным относятся также шикимовая, гликолевая, фумаровая, глицериновая и винная кислоты.
Концентрации отдельных органических кислот в различных плодах и ягодах неодинаковы.
Цитрусовые плоды содержат преимущественно лимонную кислоту и небольшие количества яблочной. Содержание последней в апельсинах составляет 10–25 %, в мандаринах — до 20 %, в грейпфрутах и лимонах — до 5 % по отношению к общей кислотности. В отличие от плодов, в кожуре апельсинов содержится значительное (примерно 0,1 %) количество щавелевой кислоты.
Лимонная кислота оказывается основной также в кислотном спектре ананасов, где ее содержание достигает 85 %. На долю яблочной кислоты в этих плодах приходится около 10 %.
Доминирующей кислотой в составе семечковых и косточковых плодов является яблочная, содержание которой в их кислотном спектре колеблется от 50 до 90 %.
В кислых сортах яблок яблочная кислота составляет свыше 90 % общей кислотности, в черешне и вишне ее концентрация достигает 85–90 %, в сливах (в зависимости от сорта) — от 35 до 90 %. В числе других кислот в этих плодах — лимонная и хинная.
Более 90 % кислотности приходится на яблочную, лимонную и хинную кислоты в таких плодах, как персики и абрикосы, причем соотношение яблочной и лимонной кислот может колебаться в широком диапазоне, что в некоторых случаях связывают с изменением содержания этих кислот в плодах в процессе созревания. Установлено, например, что при созревании персиков количество яблочной кислоты в них значительно возрастает, а лимонной — уменьшается.
В отличие от других видов плодов, в винограде основной является винная кислота, составляющая 50–65 % общей кислотности. Остаток приходится на яблочную (25–30 %) и лимонную (до 10 %) кислоты. В процессе созревания винограда содержание яблочной кислоты снижается интенсивнее, чем винной.
В большинстве видов ягод, за исключением винограда, крыжовника, черники и ежевики, преобладает лимонная кислота. Например, в землянике на ее долю приходится 70–90 %, в смородине — 85–90 %. Содержание яблочной кислоты в этих ягодах — 10–15 %. В ежевике 65–85 % составляет изолимонная кислота, а в составе крыжовника — 45 % яблочной и лимонной и 5–10 % шикимовой.
Некоторое количество кислот в плодах и ягодах может находиться в виде солей. Их содержание, например, в лимонах составляет до 3 %, а в отдельных видах груш — 20–30 %.
В отличие от большинства органических кислот, в составе плодов и ягод молочная кислота образуется только микробиологическим путем.
Кислотный спектр овощей представлен преимущественно теми же органическими кислотами, соотношение которых колеблется в значительных пределах. Наряду с уже известными в составе овощей обнаруживаются янтарная, фумаровая, пироглутаминовая и некоторые другие кислоты различного строения.
Отличительной особенностью томатов является присутствие в них неорганических кислот — фосфорной, серной и соляной.
В составе молока и молочных продуктов основной органической кислотой является молочная кислота, образование которой связано с биохимическим превращением молочного сахара — лактозы (формула лактозы приведена в п. 1) под действием молочнокислых бактерий, происходящим в соответствии с уравнением реакции
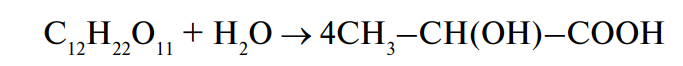
При участии в этом процессе гомоферментативных молочнокислых бактерий молочная кислота является практически единственным продуктом реакции. В случае гетероферментативных ароматообразующих молочнокислых бактерий наряду с молочной появляются уксусная и пропионовая кислоты, а также другие продукты брожения — этанол, диацетил, этилуксусный эфир.
2. Пищевые кислоты и кислотность продуктов
Кислый вкус пищевого продукта обусловливают ионы водорода, образующиеся в результате электролитической диссоциации содержащихся в нем кислот и кислых солей. Активность ионов водорода (активная кислотность) характеризуется показателем рН (отрицательный логарифм концентрации водородных ионов). Значения рН для некоторых жидких пищевых продуктов представлены ниже:
- Апельсиновый сок 3,2–3,5
- Ананасовый сок 3,6
- Виноградный сок 3,2
- Грейпфрутовый сок 3,1
- Банановый нектар 3,6–3,7
- Пиво 4,2–4,6
- Цельное молоко 6,6–6,8
- Сгущенное молоко 6,1–6,4
- Йогурт 4,0–4,3
- Какао (напиток) 6,3–6,4
Практически все пищевые кислоты являются слабыми и в водных растворах диссоциируют незначительно (константы диссоциации см. в табл. 3). Кроме того, в пищевой системе могут находиться буферные вещества, в присутствии которых активность ионов водорода будет сохраняться примерно постоянной из-за ее связи с равновесием диссоциации слабых электролитов. Примером такой системы является молоко.
Таблица 3. Свойства основных пищевых кислот
| Кислота | Эмпирическая
формула |
Молекулярная
масса |
Температура
плавления,°C |
Растворимость,
г/100 мл Н2О при 25°С |
Константа
диссоциации |
Показатель
константы кислотности рКа, при 25°С |
| Уксусная | С2Н4О2 | 60,05 | 16,75 | Смешивается | 1,76 · 10-5 | 4,75 |
| Молочная | С3Н6О3 | 90,08 | 16,8 | Хорошо
растворим |
1,37 · 10-4 | 3,86 |
| Лимонная | С6Н8О7 | 192,12 | 153
(безв.) |
181,0 | К1 = 7,1 · 10-4 | 3,14 (при +20°С) |
| К2=1,68 · 10-5 | 4,77 (при +20°С) | |||||
| К3 = 6,4 · 10-7 | 6,39 (при +20°С) | |||||
| Яблочная | С4Н6О5 | 134,09 | 132 | 62,0 | К1 = 3,9 · 10-4 | 3,40 |
| К2 = 7,8 · 10-6 | 5,11 | |||||
| Винная | С4Н6О6 | 150,09 | 168-170 | 147,0 | К1 = 1,04 · 10-3 | 2,98 |
| К2 = 4,55 · 10-5 | 4,34 | |||||
| Янтарная | С4Н6О4 | 118,09 | 188 | 6,8 | К1 = 6,5 · 10-5 | 4,21 |
| К2 = 2,3 · 10-6 | 5,64 | |||||
| Янтарный
ангидрид |
С4Н4О3 | 100,07 | 118,3 | Малорастворим | К1= 6,5 · 10-5 | |
| К2 = 2,3 · 10-6 | ||||||
| Адипиновая | С6Н10О4 | 146,14 | 152 | 1,9 (при +20°С) | К1 =3,71 · 10-5 | 4,43 |
| К2 = 3,87 · 10-6 | 5,41 | |||||
| Фумаровая | С4Н4О4 | 116,07 | 286 | 0,5 (при +20°С) | К1 = 9,3 · 10-4 (при + 18°С) | 3,03 (при +18°С) |
| К2 = 3,62 · 10-5(при +18°С) | 4,44 (при + 18°С) | |||||
| Глюконодельта-лактон | С6Н10О6 | 178,14 | 153 | 59,0 | К1 = 1,99 · 10-4 (для кислоты) | 3,70 (для кислоты) |
| Фосфорная | H3РО4 | 98,00 | 42,35 | Хорошо растворим в горячей воде | К1 = 7,52 · 10-3 | 2,12 |
| К2 = 6,23 · 10-8 | 7,21 | |||||
| К3 = 2,2 · 10-13 (при +18°С) | 12,67 |
В связи с этим суммарная концентрация в пищевом продукте веществ, имеющих кислотный характер, определяется показателем потенциальной, общей или титруемой (раствором щелочи) кислотности. Для разных продуктов эта величина выражается через различные показатели. Например, в соках определяют общую кислотность в граммах на 1 л, в молоке — в градусах Тернера и т. д.
3. Пищевые кислоты и их влияние на качество продуктов
Пищевые кислоты в составе продовольственного сырья и продуктов выполняют различные функции, связанные с качеством пищевых объектов.
В составе комплекса вкусоароматических веществ они участвуют в формировании вкуса и аромата, принадлежащих к числу основных показателей качества пищевого продукта. Именно вкус наряду с запахом и внешним видом по сей день оказывает более существенное влияние на выбор потребителем того или иного продукта по сравнению с такими показателями, как состав и пищевая ценность. Изменения вкуса и аромата часто оказываются признаками начинающейся порчи пищевого продукта или наличия в его составе посторонних веществ.
Главное вкусовое ощущение, вызываемое присутствием кислот в составе продукта, — кислый вкус, который в общем случае пропорционален концентрации ионов Н+ (с учетом различий в активности веществ, вызывающих одинаковое вкусовое восприятие). Например, пороговая концентрация (минимальная концентрация вкусового вещества, воспринимаемая органами чувств), позволяющая ощутить кислый вкус, составляет для лимонной кислоты 0,017 %, для уксусной — 0,03 %.
В случае органических кислот на восприятие кислого вкуса оказывает влияние и анион молекулы. В зависимости от природы последнего могут возникать комбинированные вкусовые ощущения, например лимонная кислота имеет острый, чистый кисло-сладкий вкус, а пикриновая — кисло-горький, яблочная кислота обладает мягким кислым вкусом, который проявляется постепенно и сохраняется в течение некоторого времени; такой же «тянущийся» кислый вкус характерен для фумаровой кислоты. Для уксусной кислоты характерен свой, типичный вкус уксуса. Большинство кислот влияет на восприятие сладости сахара. Изменение вкусовых ощущений происходит и в присутствии солей органических кислот. Так, соли аммония придают продукту соленый вкус.
Естественно, что наличие в составе продукта нескольких органических кислот в сочетании с вкусовыми органическими веществами других классов обусловливает формирование оригинальных вкусовых ощущений, часто присущих исключительно одному, конкретному виду пищевых продуктов.
Участие органических кислот в образовании аромата в различных продуктах неодинаково.
Доля органических кислот и их лактонов в комплексе ароматообразующих веществ, например, земляники составляет 14 %, в помидорах — порядка 11 %, в цитрусовых и пиве — порядка 16 %, в хлебе — более 18 %, тогда как в формировании аромата кофе на кислоты приходится менее 6 %.
В состав ароматообразующего комплекса кисломолочных продуктов входят молочная, лимонная, уксусная, пропионовая и муравьиная кислоты. Качество пищевого продукта представляет собой интегральную величину, включающую, помимо органолептических свойств (вкуса, цвета, аромата), показатели, характеризующие его коллоидную, химическую и микробиологическую стабильность.
Формирование качества продукта осуществляется на всех этапах технологического процесса его получения. При этом многие технологические показатели, обеспечивающие создание высококачественного продукта, зависят от активной кислотности (рН) пищевой системы.
В общем случае величина рН оказывает влияние на следующие технологические параметры:
- образование компонентов вкуса и аромата, характерных для конкретного вида продукта;
- коллоидную стабильность полидисперсной пищевой системы (например, коллоидное состояние белков молока или комплекса белково-дубильных соединений в пиве);
- термическую стабильность пищевой системы (например, термоустойчивость белковых веществ молочных продуктов, зависящую от состояния равновесия между ионизированным и коллоидно распределенным фосфатом кальция);
- биологическую стойкость (например, пива и соков);
- активность ферментов;
- условия роста полезной микрофлоры и ее влияние на процессы созревания (например, пива или сыров).
4. Регуляторы кислотности пищевых систем
Наличие пищевых кислот в продукте может являться следствием преднамеренного введения кислоты в пищевую систему в ходе технологического процесса для регулирования ее рН.
В этом случае пищевые кислоты используются в качестве технологических пищевых добавок.
Обобщенно можно выделить три основные цели добавления кислот в пищевую систему:
- придание определенных органолептических свойств (вкуса, цвета, аромата), характерных для конкретного продукта;
- влияние на коллоидные свойства, обусловливающие формирование консистенции, присущей конкретному продукту;
- повышение стабильности, обеспечивающей сохранение качества продукта в течение определенного времени.
В табл. 3 были приведены свойства важнейших пищевых кислот, применяемых для регулирования рН в пищевых системах и обеспечивающих ему физическую стабильность. К ним также относятся: влияние на устойчивость дисперсных систем (эмульсий и суспензий), изменение вязкости в присутствии загустителя, формирование гелевой структуры в присутствии гелеобразователя, влияние на микрофлору, обеспечивающее биологическую стойкость продукта.
Уксусная кислота (ледяная) Е260 является наиболее известной пищевой кислотой и выпускается в виде эссенции, содержащей 70–80 % собственно кислоты. В быту используют разбавленную водой уксусную эссенцию, получившую название столовый уксус. Использование уксуса для консервирования пищевых продуктов — один из наиболее старых способов консервирования. В зависимости от сырья, из которого получают уксусную кислоту, различают винный, фруктовый, яблочный, спиртовой уксус и синтетическую уксусную кислоту. Уксусную кислоту получают путем уксуснокислого брожения. Соли и эфиры этой кислоты называются ацетатами. В качестве пищевых добавок используются ацетаты калия и натрия (Е261 и Е262).
Наряду с уксусной кислотой и ацетатами применение находят диацетаты натрия и калия. Эти вещества состоят из уксусной кислоты и ацетатов в молярном соотношении 1 : 1. Уксусная кислота — бесцветная жидкость, смешивающаяся с водой во всех отношениях. Диацетат натрия — белый кристаллический порошок, растворимый в воде, с сильным запахом уксусной кислоты.
Уксусная кислота не имеет законодательных ограничений; ее действие основанное на снижении рН консервируемого продукта, проявляется при содержании выше 0,5 % и направлено главным образом против бактерий. Основная область использования — овощные консервы и маринованные продукты. Применяется в майонезах, соусах, при мариновании рыбной продукции и овощей, ягод и фруктов. Уксусная кислота широко используется как вкусовая добавка.
Молочная кислота выпускается в двух формах, отличающихся концентрацией: 40 %-ный раствор и концентрат, содержащий не менее 70 % кислоты. Получают молочнокислым брожением сахаров. Ее соли и эфиры называются лактатами. В виде пищевой добавки Е270 используется в производстве безалкогольных напитков, карамельных масс, кисломолочных продуктов. Проявляет антимикробную активность. Молочная кислота имеет ограничения к применению в продуктах детского питания.
Лимонная кислота — продукт лимоннокислого брожения сахаров. Имеет наиболее мягкий вкус по сравнению с другими пищевыми кислотами и не оказывает раздражающего действия на слизистые оболочки пищеварительного тракта. Соли и эфиры лимонной кислоты — цитраты. На долю лимонной кислоты приходится около 60 % количества всех кислот, используемых в технологии пищевых продуктов. Применяется в кондитерской промышленности, в технологии плавленых сыров, при производстве безалкогольных напитков и различных консервированных продуктов, в частности некоторых видов рыбных консервов (пищевая добавка Е330).
Яблочная кислота обладает менее кислым вкусом, чем лимонная и винная. Для промышленного использования эту кислоту получают синтетическим путем из малеиновой кислоты, в связи с чем критерии чистоты включают ограничения по содержанию в ней примесей токсичной малеиновой кислоты. Соли и эфиры яблочной кислоты называются малатами. Яблочная кислота обладает химическими свойствами оксикислот. При нагревании до 100 °С превращается в ангидрид. Применяется в кондитерской промышленности и при производстве безалкогольных напитков (добавка Е296).
Винная кислота является продуктом переработки отходов виноделия (винных дрожжей и винного камня). Не обладает каким-либо существенным раздражающим действием на слизистые оболочки желудочно-кишечного тракта и не подвергается обменным превращениям в организме человека. Основная часть (около 80 %) разрушается в кишечнике под действием бактерий. Соли и эфиры винной кислоты называются тартратами. Применяется в кондитерских изделиях, фруктовых джемах и желе, в безалкогольных напитках. Обладает способностью маскировать горький привкус интенсивных подсластителей (пищевая добавка Е334).
Янтарная кислота представляет собой побочный продукт производства адипиновой кислоты. Известен также способ ее выделения из отходов янтаря. Обладает химическими свойствами, характерными для дикарбоновых кислот, образует соли и эфиры, которые получили название сукцинаты. При 235 °С янтарная кислота отщепляет воду, превращаясь в янтарный ангидрид. Используется в пищевой промышленности для регулирования рН пищевых систем (пищевая добавка Е363).
Янтарный ангидрид является продуктом высокотемпературной дегидратации янтарной кислоты. Получают также каталитическим гидрированием малеинового ангидрида. Плохо растворим в воде, где очень медленно гидролизуется в янтарную кислоту.
Адипиновая кислота получается в промышленности главным образом двухстадийным окислением циклогексана. Обладает всеми химическими свойствами, характерными для карбоновых кислот, в частности образует соли, большинство из которых растворимы в воде. Легко этерифицируется в моно- и диэфиры. Соли и эфиры адипиновой кислоты получили название адипинаты. Является пищевой добавкой (Е355), обеспечивающей кислый вкус продуктов, в частности безалкогольных напитков.
Фумаровая кислота содержится во многих растениях и грибах, образуется при брожении углеводов в присутствии Aspergillus fumaricus. Промышленный способ получения основан на изомеризации малеиновой кислоты под действием НСl, содержащей бром. Соли и эфиры называются фумаратами. В пищевой промышленности фумаровую кислоту используют как заменитель лимонной и винной кислот (пищевая добавка Е297). Обладает токсичностью, в связи с чем суточное потребление с продуктами питания лимитировано уровнем 6 мг на 1 кг массы тела.
Глюконо-дельта-лактон — продукт ферментативного аэробного окисления β-D-глюкозы. В водных растворах глюконо-дельта-лактон гидролизуется в глюконовую кислоту, что сопровождается изменением рН раствора. Используется в качестве регулятора кислотности и разрыхлителя (пищевая добавка Е575) в десертных смесях и продуктах на основе мясных фаршей, например в сосисках.
Фосфорная кислота и ее соли — фосфаты (калия, натрия и кальция) — широко распространены в пищевом сырье и продуктах его переработки. Объемы применения в пищевых технологиях составляют около 25 % от общего количества используемых кислот. В отличие от органических кислот, фосфорная кислота не придает пищевым продуктам выраженного вкуса. Соли фосфорной кислоты могут быть кислыми или основными и проявлять буферные свойства: однозамещенный фосфат натрия используется как регулятор кислотности, ди- и тризамещенный фосфаты натрия применяются с целью повышения pH, комбинации фосфатов в буферных системах. В растворе фосфаты, имеющие отрицательный заряд, способны взаимодействовать с катионами и другими положительно заряженными группами, например, белков, полисахаридов и других молекул.
В высоких концентрациях фосфаты содержатся в молочных, мясных и рыбных продуктах, в некоторых видах злаков и орехов. В технологии молочных продуктов фосфаты обеспечивают стабильность белков при тепловой обработке, при изготовлении плавленых сыров — эмульгирование дисперсной системы, а в технологии мясных изделий с помощью фосфатов достигается стабилизация цвета изделий, сокращение потерь влаги в ходе обработки. Фосфаты (пищевые добавки Е339–Е341) вводятся в безалкогольные напитки (кока-колу) и кондитерские изделия. Функции фосфатов в пищевых продуктах могут быть различны: они способны связывать ионы металлов, увеличивать связывание воды, проявлять буферные свойства, осуществлять коррекцию рН, обеспечивать защиту порошков от слеживания и комкования, взаимодействовать с белками и другими гидроколлоидами, молекулы которых способны к диссоциации. Допустимая суточная доза в пересчете на фосфорную кислоту соответствует 5–15 мг на 1 кг массы тела (поскольку избыточное количество ее в организме может стать причиной дисбаланса кальция и фосфора).
5. Пищевые кислоты в питании
Значение пищевых кислот в питании человека определяется их энергетической ценностью и участием в обмене веществ. Коэффициент энергетической ценности (в ккал/г):
- Лимонная кислота 2,5
- Яблочная кислота 2,4
- Молочная кислота 3,6
Обычно они не вызывают дополнительной кислотной нагрузки в организме, окисляясь при обмене веществ с большой скоростью.
Основная функция органических кислот, входящих в состав пищи, связана с участием в процессах пищеварения.
К таким функциям органических кислот относятся:
- активация перистальтики кишечника;
- стимуляция секреции пищеварительных соков;
- влияние на формирование определенного состава микрофлоры путем снижения рН среды;
- торможение развития гнилостных процессов в толстом кишечнике.
Для различных органических кислот обнаружены некоторые другие эффекты воздействия.
Показано, что отдельные пищевые кислоты, например лимонная, препятствуют образованию в организме канцерогенных нитрозаминов, способствуют снижению риска возникновения и развития онкологических патологий. Лимонная кислота (соответственно цитрат) способствует также усвоению организмом кальция (ее содержание в костях и зубах составляет 0,5–1,5 %), оказывает активирующее или ингибирующее действие на некоторые ферменты. Бензойная кислота обладает антисептическим действием.
Однако, с другой стороны, известно, например, что щавелевая кислота в виде кальциевой соли способна откладываться в суставах или в виде камней — в мочевыводящих путях. Основными пищевыми источниками этой кислоты являются зеленый крыжовник, листья шпината, щавеля и крапивы. В противоположность этому в процессах, предотвращающих выпадение солей кальция в мочеточниках, важную роль играет цитрат мочевины. Образование комплексов с кальцием и магнием лежит также в основе процесса торможения кровотечения. Винная кислота организмом человека не усваивается.
6. Методы определения кислот в пищевых продуктах
В основе определения рН различных пищевых систем лежат стандартные методы, описанные в руководствах по аналитической химии. К ним относятся калориметрический и электрометрический методы.
Определение потенциальной кислотности, характеризующей общее содержание веществ, имеющих кислотный характер, основано на титровании этих веществ сильными основаниями (щелочами). Для различных пищевых продуктов характерны свои особые условия титрования, результаты которых представляют в соответствующих кислотных числах.
Анализ кислотного состава пищевого продукта дает возможность обнаружить фальсификацию или подтвердить его натуральность. Для определения содержания органических кислот используют как стандартные, так и альтернативные методы контроля.
Официальный метод анализа молочной кислоты основан на ее окислении перманганатом калия до уксусного альдегида, который определяют йодометрически. Наиболее известные методы определения винной кислоты базируются на щелочном титровании выпадающего винного камня. Большинство органических кислот можно определить хроматографическими методами.
К альтернативным относятся методы, основанные на использовании ферментативных систем. Характерными особенностями ферментативного анализа являются специфичность, обеспечивающая достоверность результатов, высокие точность и чувствительность.
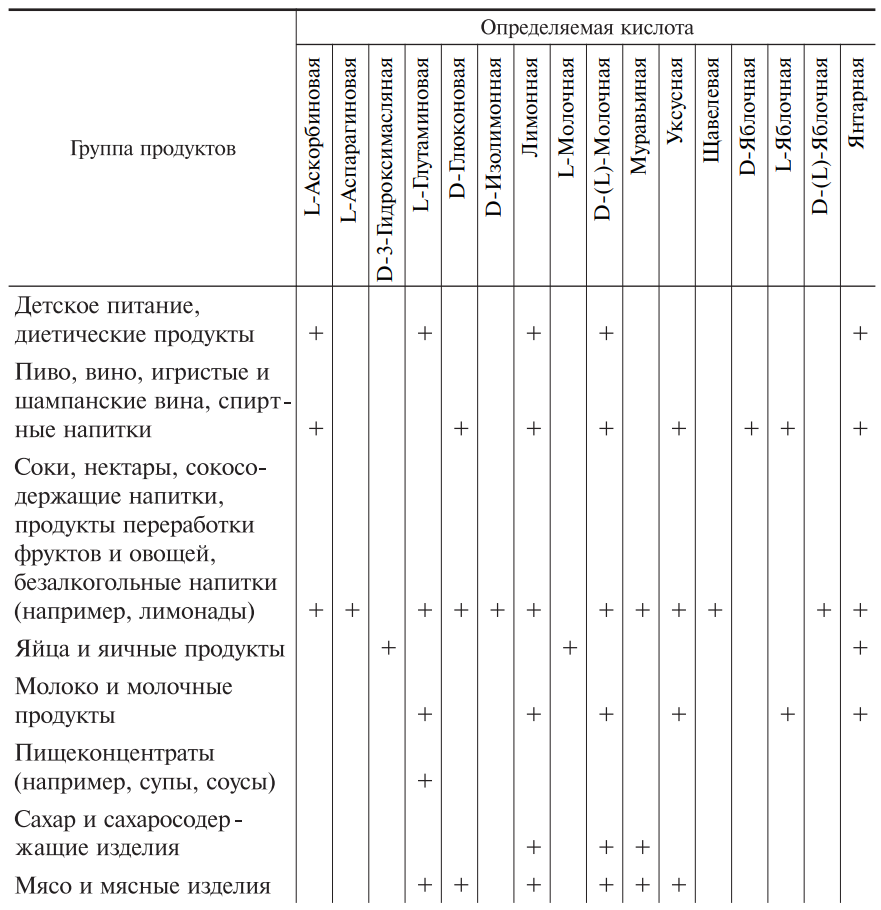
Перечень органических кислот в составе пищевых продуктов, определяемых ферментативными методами, представлен в табл. 4.
Использование ферментативных методов в аналитической химии органических пищевых кислот, в зависимости от группы анализируемых продуктов, может иметь различные цели, к которым относятся:
- производственный контроль;
- системы обеспечения качества;
- контроль качества готовой продукции;
- контроль сырья;
- оценка качества;
- анализ состава с целью установления пищевых свойств и их соответствия нормативной документации;
- оценка гигиенического статуса;
- мониторинг качества;
- выявление нежелательных компонентов;
- установление фальсификации;
- определение доли натурального сырья;
- определение аутентичности (подлинности).
Таблица 4. Пищевые кислоты в составе различных продуктов питания, определяемые ферментативными методами