Содержание страницы
1. Роль минеральных веществ в организме человека
Многие элементы в виде минеральных солей, ионов, комплексных соединений и органических веществ входят в состав живой материи и являются незаменимыми нутриентами, которые должны ежедневно потребляться с пищей. Содержание минеральных веществ в основных продуктах питания приведено в табл. 1.
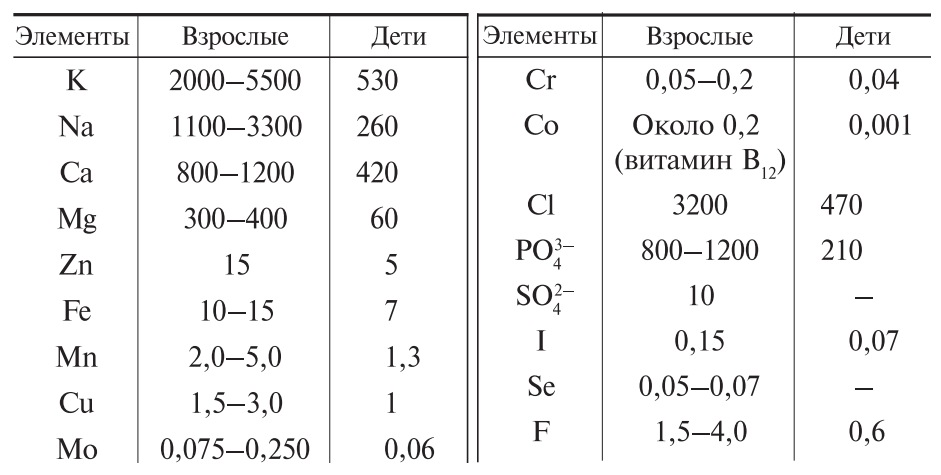
В соответствии с рекомендацией диетологической комиссии Национальной академии США ежедневное поступление химических элементов с пищей должно находиться на определенном уровне (табл. 2). Столько же химических элементов должно ежесуточно выводиться из организма, поскольку их содержание в нем находится в относительном постоянстве.
Роль минеральных веществ в организме человека чрезвычайно разнообразна, несмотря на то что они не являются обязательным компонентом питания. Минеральные вещества содержатся в протоплазме и биологических жидкостях, играют основную роль в обеспечении постоянства осмотического давления, что является необходимым условием для нормальной жизнедеятельности клеток и тканей. Они входят в состав сложных органических соединений (например, гемоглобина, гормонов, ферментов), являются пластическим материалом для построения костной и зубной ткани. В виде ионов минеральные вещества участвуют в передаче нервных импульсов, обеспечивают свертывание крови и другие физиологические процессы организма.
Таблица 1. Минеральный состав основных продуктов питания (по данным И. М. Скурихина, М. Н. Волгарева, «Химический состав пищевых продуктов», 1987)
| Пищевые продукты | Макроэлементы, мг | Микроэлементы, мкг | ||||||||||||||
| Kа-лий | Kаль-ций | Маг-ний | Нат-рий | Сера | Фос-фор | Хлор | Же-лезо | Иод | Kо-бальт | Мар-ганец | Медь | Фтор | Хром | Цинк | Молиб-ден | |
| Хлеб: | ||||||||||||||||
| ржаной формовой | 245 | 35 | 47 | 610 | 52 | 158 | 980 | 3900 | 5,6 | — | 1610 | 220 | 35 | 2,7 | 1210 | 8 |
| формовой из пшеничной муки I сорта | 129 | 23 | 33 | 506 | 59 | 84 | 837 | 1860 | — | 1,8 | 825 | 134 | — | 2,2 | 735 | 12,8 |
| Молочные продукты: | ||||||||||||||||
| молоко коровье | 146 | 120 | 14 | 50 | 29 | 90 | 110 | 67 | 9 | 0,8 | 6 | 12 | 20 | 2 | 400 | 5 |
| творог жирный | 112 | 150 | 23 | 41 | — | 216 | — | 461 | — | — | 8 | 74 | — | — | 394 | — |
| сыр российский | 116 | 1000 | 50 | 820 | — | 540 | — | 1100 | — | — | — | 50 | — | — | 3500 | — |
| Мясо: | ||||||||||||||||
| свинина | 316 | 8 | 27 | 64,8 | 220 | 170 | 48 | 1940 | 6,6 | 8 | 28,5 | 96 | 69 | 13,5 | 2070 | 13 |
| говядина | 355 | 10,2 | 22 | 73 | 230 | 188 | 59 | 2900 | 7,2 | 7 | 35 | 182 | 63 | 8,2 | 3240 | 11,6 |
| баранина | 329 | 9,8 | 25,1 | 101 | 165 | 168 | 83,6 | 2090 | 2,7 | 6 | 35 | 238 | 120 | 8,7 | 2820 | 9 |
| Рыба: | ||||||||||||||||
| речной карп | 265 | 35 | 25 | 55 | 180 | 210 | 55 | 800 | 5 | 35 | 150 | 130 | 25 | 55 | 2080 | 4 |
| морская треска | 340 | 25 | 30 | 100 | 200 | 210 | 165 | 650 | 135 | 30 | 80 | 150 | 700 | 55 | 1020 | 4 |
| Овощи: | ||||||||||||||||
| капуста белокочанная | 185 | 48 | 16 | 13 | 37 | 31 | 37 | 600 | 3 | 3 | 170 | 75 | 10 | 5 | 400 | 10 |
| картофель | 568 | 10 | 23 | 28 | 32 | 58 | 58 | 900 | 5 | 5 | 170 | 140 | 30 | 10 | 360 | 8 |
| морковь | 200 | 51 | 38 | 21 | 6 | 55 | 63 | 700 | 5 | 2 | 200 | 80 | 55 | 3 | 400 | 20 |
| Фрукты: | ||||||||||||||||
| слива | 214 | 20 | 9 | 18 | 6 | 20 | 1 | 500 | 4 | 1 | 110 | 87 | 2 | 4 | 100 | 8 |
| яблоко | 278 | 16 | 9 | 26 | 5 | 11 | 2 | 2200 | 2 | 1 | 47 | 110 | 8 | 4 | 150 | 6 |
Таблица 2. Суточное поступление химических элементов в организм человека (в мг) [Ю. Н. Кукушкин, 1998]
В зависимости от количества минеральных веществ в организме человека и пищевых продуктах их подразделяют на макро- и микроэлементы. Так, если массовая доля элемента в организме превышает 10–2 %, то его следует считать макроэлементом. Доля микроэлементов в организме составляет 10–3–10–5 %. Если содержание элемента ниже 10–5 %, его считают ультрамикроэлементом.
К макроэлементам относят калий, натрий, кальций, магний, фосфор, хлор и серу. Они содержатся в количествах, измеряемых сотнями и десятками миллиграммов на 100 г тканей или пищевого продукта.
Микроэлементы входят в состав тканей организма в концентрациях, выражаемых десятыми, сотыми и тысячными долями миллиграмма и являются необходимыми для его нормальной жизнедеятельности.
Микроэлементы условно делят на две группы: абсолютно, или жизненно необходимые (кобальт, железо, медь, цинк, марганец, йод, бром, фтор) и так называемые вероятно необходимые (алюминий, стронций, молибден, селен, никель, ванадий и некоторые другие).
Микроэлементы называют жизненно необходимыми, если при их отсутствии или недостатке нарушается нормальная жизнедеятельность организма. Характерным признаком необходимого элемента является колоколообразный вид кривой зависимости ответной реакции организма от дозы элемента (рис. 1).
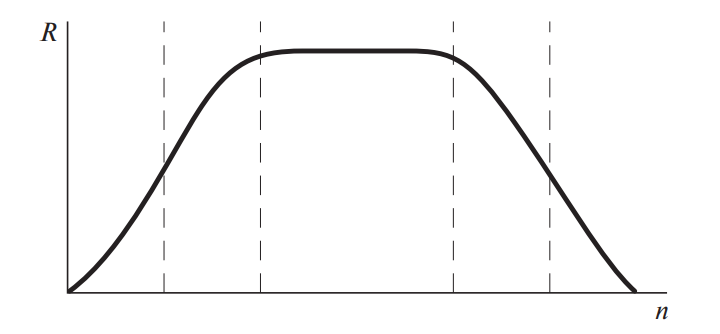
Рис. 1. Зависимость ответной реакции (R) от дозы (n) жизненно необходимых элементов
При малом поступлении данного элемента организму наносится существенный ущерб. Он функционирует на грани выживания. В основном это объясняется снижением активности ферментов, в состав которых входит данный элемент. При повышении дозы элемента ответная реакция возрастает и достигает нормы (на кривой представлена в виде плато). При дальнейшем увеличении дозы проявляется токсическое действие избытка данного элемента, в результате чего не исключается и летальный исход.
Распределение микроэлементов в организме зависит от их химических свойств и оно очень разнообразно. Железо, например, является составной частью гемоглобина, миоглобина и других дыхательных пигментов, то есть веществ, участвующих в поглощении и транспорте кислорода во все ткани организма; атомы меди входят в активный центр ряда ферментов и т. д.
Действие микроэлементов может быть и опосредованным — через влияние на интенсивность или характер обмена веществ. Так, некоторые микроэлементы (например, марганец, цинк, йод) влияют на рост, и их недостаточное поступление в организм с пищей тормозит нормальное физическое развитие ребенка. Другие микроэлементы (например, молибден, медь, марганец) принимают участие в репродуктивной функции, и их недостаток в организме отрицательно влияет на эту сторону жизнедеятельности человека.
К наиболее дефицитным минеральным веществам в питании современного человека относятся кальций и железо, к избыточным — натрий и фосфор.
Недостаток или избыток в питании каких-либо минеральных веществ вызывает нарушение обмена белков, жиров, углеводов, витаминов, что приводит к развитию ряда заболеваний. Ниже приведены характерные (типичные) симптомы при дефиците различных химических элементов в организме человека:

Наиболее распространенным следствием несоответствия в рационе количества кальция и фосфора является кариес зубов, разрежение костной ткани. При недостатке фтора в питьевой воде разрушается зубная эмаль, дефицит йода в пище и воде приводит к заболеваниям щитовидной железы. Таким образом, минеральные вещества очень важны для устранения и профилактики ряда заболеваний.
Перечислим причины нарушения обмена минеральных веществ, которые могут иметь место даже при их достаточном количестве в пище:
- а) несбалансированное питание (недостаточное или избыточное количество белков, жиров, углеводов, витаминов и др.);
- б) применение методов кулинарной обработки пищевых продуктов, обусловливающих потери минеральных веществ, например, при размораживании (в горячей воде) мяса, рыбы или при удалении отваров овощей и фруктов, куда переходят растворимые соли;
- в) отсутствие своевременной коррекции состава рационов при изменении потребности организма в минеральных веществах, связанной с физиологическими причинами. Так, например, у людей, работающих в условиях повышенной температуры внешней среды, увеличивается потребность в калии, натрии, хлоре и других минеральных веществах в связи с тем, что большая их часть выводится из организма с потом;
- г) нарушение процесса всасывания минеральных веществ в желудочно-кишечном тракте или повышение потерь жидкости (например, кровопотери).
2. Роль отдельных минеральных элементов
2.1. Макроэлементы
Кальций. Это основной структурный компонент костей и зубов; входит в состав ядер клеток, клеточных и тканевых жидкостей, необходим для свертывания крови. Кальций образует соединения с белками, фосфолипидами, органическими кислотами, участвует в регуляции проницаемости клеточных мембран, в процессах передачи нервных импульсов, в молекулярном механизме мышечных сокращений, контролирует активность ряда ферментов. Таким образом, кальций выполняет не только пластические функции, но и влияет на многие биохимические и физиологические процессы в организме.
Кальций относится к трудноусвояемым элементам. Поступающие в организм человека с пищей соединения кальция практически нерастворимы в воде. Щелочная среда тонкого кишечника способствует образованию трудноусвояемых соединений кальция, и лишь воздействие желчных кислот обеспечивает его всасывание.
Ассимиляция кальция тканями зависит не только от содержания его в продуктах, но и от соотношения его с другими компонентами пищи, в первую очередь с жирами, магнием, фосфором, белками. При избытке жиров возникает конкуренция за желчные кислоты и значительная часть кальция выводится из организма через толстый кишечник. На всасывание кальция отрицательно сказывается избыток магния; рекомендуемое соотношение этих элементов составляет 1 : 0,5.
Если количество фосфора превышает уровень кальция в пище более чем в 2 раза, то образуются растворимые соли, которые извлекаются кровью из костной ткани. Кальций поступает в стенки кровеносных сосудов, что обусловливает их ломкость, а также в ткани почек, что может способствовать возникновению почечно-каменной болезни. Для взрослых рекомендовано соотношение кальция и фосфора в пище 1 : 1,5. Трудность соблюдения такого соотношения обусловлена тем, что большинство широко потребляемых продуктов значительно богаче фосфором, чем кальцием. Отрицательное влияние на усвоение кальция оказывает фитин и щавелевая кислота, содержащиеся в ряде растительных продуктов. Эти соединения образуют с кальцием нерастворимые соли.
Суточная потребность в кальции взрослого человека составляет 800 мг, а у детей и подростков — 1000 мг и более.
При недостаточном потреблении кальция или при нарушении всасывания его в организме (при недостатке витамина D) развивается состояние кальциевого дефицита. Наблюдается повышенное выведение его из костей и зубов. У взрослых развивается остеопороз — деминерализация костной ткани, у детей нарушается становление скелета, развивается рахит.
Лучшими источниками кальция являются молоко и молочные продукты, различные сыры и творог (100–1000 мг/100 г продукта), зеленый лук, петрушка, фасоль. Значительно меньше кальция содержится в яйцах, мясе, рыбе, овощах, фруктах, ягодах (20–40 мг/100 г продукта).
Магний. Этот элемент необходим для активности ряда ключевых ферментов, обеспечивающих метаболизм организма. Магний участвует в поддержании нормальной функции нервной системы и мышцы сердца, оказывает сосудорасширяющее действие, стимулирует желчеотделение, повышает двигательную активность кишечника, что способствует выведению шлаков из организма (в том числе холестерина).
Усвоению магния мешают наличие фитина и избыток жиров и кальция в пище.
Ежедневная потребность в магнии точно не определена; считают, однако, что доза 200–300 мг/сут предотвращает проявление его недостаточности (предполагается, что всасывается около 30 % магния). Известны случаи врожденной недостаточности всасывания магния из кишечника, что указывает на наличие специфического механизма всасывания этого иона. При недостатке магния нарушается усвоение пищи, задерживается рост, в стенках сосудов откладывается кальций, развивается ряд других патологических явлений.
У человека недостаток ионов магния, обусловленный характером питания, крайне маловероятен. Однако большие потери этого элемента могут происходить при диарее; последствия их сказываются, если в организм вводятся жидкости, не содержащие магний. Когда концентрация магния в сыворотке снижается примерно до 0,1 ммоль/л, может возникать синдром, напоминающий белую горячку: у человека наступает полукоматозное состояние, наблюдается мышечная дрожь, спазмы мышц в области запястья и стопы, повышение нервно-мышечной возбудимости в ответ на звуковые, механические и зрительные раздражители. Введение магния вызывает быстрое улучшение состояния.
Магнием богаты в основном растительные продукты. Большое количество его содержат пшеничные отруби, различные крупы (40–200 мг/ 100 г продукта), бобовые, урюк, курага, чернослив. Мало магния в молочных продуктах, мясе, рыбе, макаронных изделиях, большинстве овощей и фруктов (20–40 мг/100 г).
Калий. Около 90 % калия находится внутри клеток. Он вместе с другими солями обеспечивает осмотическое давление, участвует в передаче нервных импульсов, регуляции водно-солевого обмена, способствует выведению воды, а следовательно, и шлаков из организма, поддерживает кислотно-щелочное равновесие внутренней среды организма, участвует в регуляции деятельности сердца и других органов, необходим для функционирования ряда ферментов.
Калий хорошо всасывается из кишечника, а его избыток быстро удаляется из организма с мочой.
Суточная потребность в калии взрослого человека составляет 2000– 4000 мг. Она увеличивается при обильном потоотделении, при употреблении мочегонных средств, заболеваниях сердца и печени.
Калий не является дефицитным нутриентом в питании, и при разнообразном питании недостаточность калия не возникает. Дефицит калия в организме появляется при нарушении функций нервно-мышечной и сердечно-сосудистой систем, сонливости, снижении артериального давления, нарушении ритма сердечной деятельности. В таких случаях назначается калиевая диета.
Большая часть калия поступает в организм с растительными продуктами. Богатыми источниками его являются урюк, чернослив, изюм, шпинат, морская капуста, фасоль, горох, картофель, другие овощи и плоды (100–600 мг/100 г продукта). Меньше калия содержится в сметане, рисе, хлебе из муки высшего сорта (100–200 мг/100 г).
Натрий. Натрий содержится во всех тканях и биологических жидкостях организма. Он участвует в поддержании осмотического давления в тканевых жидкостях и крови, в передаче нервных импульсов, регуляции кислотно-щелочного равновесия, водно-солевого обмена, повышает активность пищеварительных ферментов.
Метаболизм натрия всесторонне изучен благодаря его физиологическим свойствам и важности для организма. Этот нутриент легко всасывается из кишечника. Ионы натрия вызывают набухание коллоидов тканей, что обусловливает задержку воды в организме и противодействует ее выделению. Уровень натрия во внеклеточной жидкости тщательно поддерживается почками под влиянием эндокринных, сердечно-сосудистых и автономных регуляторных механизмов. Общее количество натрия во внеклеточной жидкости, таким образом, определяет объем этих жидкостей. Контроль за балансом натрия осуществляется посредством сложной взаимосвязанной системы, включающей нервную и гормональную системы. Возрастание концентрации натрия в плазме стимулирует осморецепторы в центре гипоталамуса независимо от объема жидкости, что приводит к ощущению жажды. В жарком климате и при тяжелой физической работе происходит существенная потеря натрия с потом, и необходимо введение в организм соли для восполнения утраченного его количества.
Обычно соли натрия не обладают острой токсичностью, поскольку полностью развитые почки эффективно выводят натрий из организма. В основном ионы натрия поступают в организм за счет поваренной соли NaCl. При избыточном потреблении хлорида натрия ухудшается удаление растворимых в воде конечных продуктов обмена веществ через почки, кожу и другие выделительные органы. Задержка воды в организме осложняет деятельность сердечно-сосудистой системы, способствует повышению кровяного давления. Поэтому потребление соли при соответствующих заболеваниях в пищевом рационе ограничивают. Вместе с тем при работе в горячих цехах или жарком климате увеличивают количество натрия (в виде поваренной соли), вводимого извне, чтобы компенсировать его потерю с потом и уменьшить потоотделение, отягощающее функцию сердца.
Натрий естественно присутствует во всех пищевых продуктах. Способ получения пищевых продуктов в значительной мере определяет конечное содержание в нем натрия. Например, замороженный зеленый горошек содержит гораздо больше натрия, чем свежий. Свежие овощи и фрукты содержат его от менее чем 10 мг/кг до 1 г/кг, в отличие от круп и сыра, которые могут содержать натрий в количестве 10–20 г/кг.
Оценка среднесуточного поступления натрия с пищей затруднена, поскольку его концентрация в пище широко варьируется и, кроме того, люди привыкли подсаливать пищу. Взрослый человек ежедневно потребляет до 15 г поваренной соли и столько же выделяет ее из организма. Это количество значительно превышает физиологически необходимое и определяется прежде всего вкусовыми качествами хлорида натрия, привычкой к соленой пище. Содержание поваренной соли в пище человека можно без ущерба для здоровья снизить до 5 г в сутки. На выделение хлорида натрия из организма, а следовательно, и на потребность в нем влияет количество солей калия, получаемое организмом. Растительная пища, особенно картофель, богата калием и усиливает выделение с мочой хлорида натрия, а следовательно, и повышает потребность в нем.
Фосфор. Фосфор входит в состав всех тканей организма, особенно мышц и мозга. Этот элемент принимает участие во всех процессах жизнедеятельности организма: синтезе и расщеплении веществ в клетках; регуляции обмена веществ; входит в состав нуклеиновых кислот и ряда ферментов; необходим для образования АТФ.
В тканях организма и пищевых продуктах фосфор содержится в виде фосфорной кислоты и ее органических соединений (фосфатов). Основная его масса находится в костной ткани в виде фосфорнокислого кальция, остальной фосфор входит в состав мягких тканей и жидкостей. В мышцах происходит наиболее интенсивный обмен соединений фосфора. Фосфорная кислота участвует в построении молекул многих ферментов, нуклеиновых кислот и т. д.
Содержание органических соединений фосфора в крови меняется в широких пределах. Однако количество неорганического фосфора более или менее постоянно. Увеличивается содержание неорганического фосфора при молочной диете, а также при ряде заболеваний почек, при переломах на стадии заживления, сахарном диабете и др.; уменьшается концентрация неорганического фосфора в сыворотке крови при повышении функции паращитовидных желез и ряде других заболеваний.
При длительном дефиците фосфора в питании организм использует собственный фосфор из костной ткани. Это приводит к деминерализации костей и нарушению их структуры — разрежению. При обеднении организма фосфором снижается умственная и физическая работоспособность, отмечается потеря аппетита, апатия.
Суточная потребность в фосфоре для взрослых составляет 1200 мг. Она возрастает при больших физических или умственных нагрузках, при некоторых заболеваниях.
Большое количество фосфора содержится в продуктах животного происхождения, особенно в печени, икре, а также в зерновых и бобовых. Его содержание в этих продуктах составляет от 100 до 500 мг в 100 г продукта. Богатым источником фосфора являются крупы (овсяная, перловая), в них содержится 300–350 мг фосфора/100 г. Однако из растительных продуктов соединения фосфора усваиваются хуже, чем при потреблении пищи животного происхождения.
Сера. Значение этого элемента в питании определяется в первую очередь тем, что он входит в состав белков в виде серосодержащих аминокислот (метионина и цистина), а также является составной частью некоторых гормонов и витаминов.
Как компонент серосодержащих аминокислот, сера участвует в процессах белкового обмена, причем потребность в ней резко возрастает в период беременности и роста организма, сопровождающихся активным включением белков в образующиеся ткани, а также при воспалительных процессах. Серосодержащие аминокислоты, особенно в сочетании с витаминами С и Е, оказывают выраженное антиоксидантное действие. Наряду с цинком и кремнием сера определяет функциональное состояние волос и кожи.
Содержание серы обычно пропорционально содержанию белков в пищевых продуктах, поэтому ее больше в животных продуктах, чем в растительных. Потребность в сере (400–600 мг в сутки) удовлетворяется обычным суточным рационом.
Хлор. Этот элемент участвует в образовании желудочного сока, формировании плазмы, активирует ряд ферментов. Этот нутриент легко всасывается из кишечника в кровь. Интересна способность хлора отлагаться в коже, задерживаться в организме при избыточном поступлении, выделяться с потом в значительных количествах. Выделение хлора из организма происходит главным образом с мочой (90 %) и по´том.
Нарушения в обмене хлора ведут к развитию отеков, недостаточной секреции желудочного сока и др. Резкое уменьшение содержания хлора в организме может привести к тяжелому состоянию, вплоть до летального исхода. Повышение его концентрации в крови наступает при обезвоживании организма, а также при нарушении выделительной функции почек.
Суточная потребность в хлоре составляет примерно 5000 мг. Хлор поступает в организм человека в основном в виде хлорида натрия при добавлении его в пищу.
2.2. Микроэлементы
Железо. Этот элемент необходим для биосинтеза соединений, обеспечивающих дыхание, кроветворение; он участвует в иммунобиологических и окислительно-восстановительных реакциях, входит в состав цитоплазмы, клеточных ядер и ряда ферментов.
Ассимиляции железа препятствует щавелевая кислота и фитин. Для усвоения этого нутриента необходим витамин В12. Усвоению железа способствует также аскорбиновая кислота, поскольку железо всасывается в виде двухвалентного иона.
Недостаток железа в организме может привести к развитию анемии, нарушаются газообмен, клеточное дыхание, то есть фундаментальные процессы, обеспечивающие жизнедеятельность организма. Развитию железодефицитных состояний способствуют: недостаточное поступление в организм железа в усвояемой форме, понижение секреторной активности желудка, дефицит витаминов (особенно В12, фолиевой и аскорбиновой кислот) и ряд заболеваний, вызывающих кровопотери.
Потребность взрослого человека в железе (14 мг/сут) с избытком удовлетворяется обычным рационом. Однако при использовании в пище хлеба из муки тонкого помола, содержащего мало железа, у городских жителей весьма часто наблюдается дефицит железа. При этом следует учесть, что зерновые продукты, богатые фосфатами и фитином, образуют с железом труднорастворимые соединения и снижают его ассимиляцию организмом.
Железо — широко распространенный элемент. Он содержится в субпродуктах, мясе, яйцах, фасоли, овощах, ягодах. Однако в легкоусвояемой форме железо содержится только в мясных продуктах, печени (до 2000 мг/100 г продукта), яичном желтке.
Медь. Медь является необходимым элементом в метаболизме человека, играя роль в образовании эритроцитов, высвобождении тканевого железа и развитии скелета, центральной нервной системы и соединительной ткани. Обычно медь соединена с белками: гемокупреном в эритроцитах и церулоплазмином в плазме крови, в которых медь является неотъемлемой частью их структуры; металлотионеин представляет собой белок, ответственный за отложение меди. Выделен ряд медьсодержащих ферментов, в частности цитохромоксидаза, оксидаза аскорбиновой кислоты и уриказа.
Поскольку медь широко распространена в пищевых продуктах, маловероятно, чтобы у людей, за исключением, возможно, грудных детей, получающих исключительно молочный рацион, когда-либо развилась форма недостаточности питания, связанная с медью.
Потребление избыточно больших доз меди человеком ведет к раздражению и разъеданию слизистых, распространенному поражению капилляров, поражению печени и почек, раздражению центральной нервной системы. Суточная потребность в этом элементе составляет около 2 мг. Источниками меди являются такие пищевые продукты, как печень, яичный желток, зеленые овощи.
Йод. Йод является необходимым элементом, участвующим в образовании гормона тироксина. При недостаточности йода развивается зобная болезнь — заболевание щитовидной железы.
Потребность в йоде колеблется в пределах 100–150 мкг в день. Содержание йода в пищевых продуктах обычно невелико (4–15 мкг%). Наиболее богаты йодом продукты моря. Так, в морской рыбе его содержится около 50 мкг/100 г, в печени трески — до 800, в морской капусте в зависимости от вида и сроков сбора — от 50 до 70 000 мкг/100 г продукта. Но надо учесть, что при длительном хранении и тепловой обработке пищи значительная часть йода (от 20 до 60 %) теряется.
Содержание йода в наземных растительных и животных продуктах сильно зависит от его количества в почве. В районах, где йода в почве мало, содержание его в пищевых продуктах может быть в 10–100 раз меньше среднего. Поэтому в этих районах для предупреждения зобной болезни добавляют в поваренную соль небольшое количество йодата калия (25 мг на 1 кг соли). Срок хранения такой йодированной соли — не более 6 месяцев, так как при хранении соли йод постепенно улетучивается.
Фтор. При недостатке этого элемента развивается кариес зубов (разрушение зубной эмали). Избыток фтора также оказывает негативное влияние на организм, поскольку соли фтора, накапливаясь в костях, вызывают изменение цвета (крапчатость) и формы зубов, остеохондроз, а вслед за этим огрубление суставов и их неподвижность, костные наросты. Разница между полезной и вредной дозами фтора так мала, что многие исследователи выступают против фторирования воды.
Фтор, потребляемый с водой, почти полностью всасывается, содержащийся в пище фтор всасывается в меньшей степени. Поглощенный фтор равномерно распределяется по всему организму. Он удерживается главным образом в скелете, и небольшое его количество отлагается в зубной ткани. В высоких дозах фтор может вызывать нарушение углеводного, липидного, белкового обмена, а также метаболизма витаминов, ферментов и минеральных солей. Многие симптомы острого отравления фтором являются следствием связывания его с кальцием. Фтор выводится из организма главным образом с мочой. На его выведение влияет ряд факторов, в том числе общее состояние здоровья человека и предшествующее воздействие на него фторидов. Степень удерживания фтора снижается с возрастом, и считается, что организм большинства взрослых находится в «состоянии равновесия», при котором присутствующий в организме фтор откладывается в обызвествленных тканях; основная часть остального количества содержится в плазме, и таким образом он становится доступным для выведения. Удержание в скелете и выведение фтора почками — два основных механизма, с помощью которых предотвращается накопление токсичных количеств фтора в организме.
В различных странах были проведены оценки суточного поступления фтора с пищей; для взрослых эта величина варьируется от 0,2 до 3,1 мг, для детей возрастной группы от 1 до 3 лет поступление фтора было оценено на уровне 0,5 мг/сут.
Практически все пищевые продукты содержат хотя бы микроколичества этого элемента. Все виды растительности содержат некоторое количество фтора, которое они получают из почвы и воды. В отдельных продуктах, в частности в рыбе, некоторых овощах и чае, обнаруживаются высокие уровни содержания фтора. Применение фторированной воды на предприятиях пищевой промышленности может нередко удваивать уровень содержания фтора в готовых продуктах.
Для профилактики и лечения кариеса зубов используют различные зубные пасты, порошки, эликсиры, жевательные резинки и т. п., которые содержат добавляемый к ним фтор, главным образом в неорганической форме. Эти соединения обычно вносятся в средства для чистки зубов, как правило, в концентрациях около 1 г/кг.
Хром. Этот элемент, по-видимому, необходим для глюкозного и липидного обмена и для утилизации аминокислот некоторыми системами. Он также имеет важное значение для профилактики легких форм диабета и атеросклероза у человека.
Хром всасывается как из желудочно-кишечного тракта, так и из дыхательных путей. Поглощаемое количество его неодинаково для каждой из этих систем и зависит от формы хрома. Трехвалентный хром является эссенциальной формой элемента для человека, шестивалентный хром токсичен. Хром распределяется по тканям человеческого организма в неодинаковых, но обычно низких концентрациях. Уровни содержания хрома во всех тканях, помимо легких, снижаются с возрастом. Наибольшие количества хрома у человека накапливаются в коже, мышцах и жировой ткани. Гомеостатические механизмы, включая механизмы транспорта в печени и кишечнике, препятствуют избыточному накоплению трехвалентного хрома. Хром медленно выводится из организма, главным образом с мочой.
Сегодня принято считать нормой потребления около 150 мг хрома в сутки. Особенно он полезен пожилым людям, организм которых плохо усваивает углеводы, а хром усиливает процессы обмена именно этих соединений. Обнаружено, что определенное соединение хрома, названное GTF (Glucose Tolerance Factor), облегчает усвоение глюкозы, вернее, проникновение ее через мембрану внутрь клеток.
Неорганический хром усваивается плохо, гораздо легче — в органических соединениях, то есть в той форме, в которой он находится в живых организмах.
У здоровых людей содержание хрома несколько завышено, что является признаком полноценного усвоения глюкозы. Если усвоение сахаров нарушено, содержание этого элемента снижается.
Продукты питания значительно варьируются по уровням содержания хрома, которые лежат в диапазоне от 20 до 550 мкг/кг. Богатыми источниками хрома являются пивные дрожжи, печень (10–80 мкг/100 г). В меньших количествах этот элемент содержится в картофеле с кожурой, говядине, свежих овощах, хлебе из муки грубого помола, сыре.
Марганец. Он является необходимым элементом для животных и человека, но из поступившего внутрь марганца всасывается лишь около 3 %. Марганец необходим как кофактор в ряде ферментных систем; он играет роль в правильном функционировании флавопротеинов, в синтезе сульфированных мукополисахаридов, холестерина, гемоглобина и во многих других процессах метаболизма.
Основными путями всасывания марганца являются дыхательный и желудочно-кишечный тракты. Вследствие слабой растворимости марганца в желудочном соке из желудочно-кишечного тракта всасывается только 3–4 % введенного количества вещества. Всасывание марганца тесно связано с усвоением железа. Анемия ведет к повышению всасывания как железа, так и марганца. Выведение марганца из организма происходит частично за счет секреции поджелудочной железы, а также непосредственно через кишечную стенку. Очень небольшое количество марганца выводится с мочой.
Потребность в марганце составляет 0,2–0,3 мг на 1 кг веса человека в день. Больше всего марганца содержится в клюкве и чае, немного меньше его в каштанах, какао, овощах, фруктах (100–200 мкг/100 г).
Никель. Никель признан незаменимым микроэлементом относительно недавно. В настоящее время установлена его роль в качестве кофермента в процессах метаболизма железа. При этом увеличение поступления в организм железа сопровождается увеличением потребности в пищевом никеле. Кроме того, никель способствует усвоению меди — еще одного незаменимого для кроветворения элемента. При экспериментальных исследованиях препаратов никеля было показано значительное ускорение регенерации эритроцитов и увеличение количества гемоглобина. Важность пищевого или выделенного из натуральных продуктов никеля подчеркивается тем, что синтетические соединения данного элемента относятся к канцерогенным веществам.
Никель присутствует в большинстве пищевых продуктов, однако в концентрациях ниже (и часто намного ниже) 1 мг/кг. Мало известно o химической форме никеля в пищевых продуктах, хотя он, возможно, частично образует комплексы с фитиновой кислотой. Поступление никеля с пищей, по имеющимся данным, варьируется от менее чем 200 до 900 мкг/сут. С обычной диетой поступает около 400 мкг/сут. Было показано, что в вине и пиве содержание никеля равно соответственно 100 и 50 мкг/л.
Цинк. Данный микроэлемент в качестве кофермента участвует в широком спектре реакций биосинтеза белка (более 70) и метаболизма нуклеиновых кислот (включая процессы репликации ДНК и транскрипции), обеспечивающих в первую очередь рост и половое созревание организма. При этом цинк наряду с марганцем является специфическим микроэлементом, влияющим на состояние половой функции, а именно на активность некоторых половых гормонов, сперматогенез, развитие мужских половых желез и вторичных половых признаков. Кроме того, в последнее время рассматривается роль цинка в предотвращении гипертрофических процессов в предстательной железе.
Цинк вместе с серой участвует в процессах роста и обновления кожи и волос. Наряду с марганцем и медью цинк в значительной степени обеспечивает восприятие вкусовых и обонятельных ощущений. Цинк в качестве незаменимого компонента входит в состав молекулы инсулина, причем уровень его оказывается сниженным у больных сахарным диабетом. Очень важно, что данный микроэлемент является коферментом алкогольдегидрогеназы, обеспечивающей метаболизм этилового спирта. При этом уровень всасываемости цинка при хроническом алкоголизме резко снижен. Необходимо также учитывать участие цинка в порфириновом обмене, тесно связанном с процессами кроветворения. Кроме того, цинк (наряду с витамином С) необходим для активации фолиевой кислоты из связанной формы, после чего фолацин может проникать внутрь клеток и включаться в процессы кроветворения.
Другая важная взаимосвязь цинка и витаминов прослеживается в отношении витамина А. Во-первых, цинк в качестве кофермента способствует высвобождению витамина А из внутрипеченочного «депо». Во-вторых, цинк необходим для трансформации ретинола (собственно витамин А) в ретиналь, который участвует в образовании зрительного пигмента сетчатки. Таким образом, так называемая «куриная слепота» (то есть нарушение ночного видения) может развиваться не только в отсутствии витамина А, но и цинка. Цинк вместе с витамином В6 обеспечивает метаболизм ненасыщенных жирных кислот и синтез простагландинов.
Цинк очень важен для процессов пищеварения и усвоения питательных веществ. Так, цинк обеспечивает синтез важнейших пищеварительных ферментов в поджелудочной железе, а также участвует в образовании хиломикронов — транспортных частиц, в составе которых пищевые жиры могут всасываться в кровь.
Цинк наряду с витаминами группы В является важным регулятором функций нервной системы. В условиях дефицита цинка могут возникать эмоциональные расстройства, эмоциональная неустойчивость, раздражительность, а в очень тяжелых случаях — нарушения функций мозжечка. Наконец, все больше данных накапливается в пользу участия цинка в процессах созревания лимфоцитов и реакциях клеточного иммунитета.
Первостепенная важность данного микроэлемента для функций организма подчеркивается тем фактом, что цинк является одним из немногих минералов, для которого описаны отдельные и совершенно специфичные синдромы недостаточности. В случае дефицита цинка развивается так называемый энтеропатический дерматит. Он особенно характерен для отдельных национальных групп, использующих в качестве основной пищи бездрожжевой хлеб, в котором в очень большом количестве обнаруживаются соли фитиновой кислоты, которые обычно разрушаются дрожжевой фитазой. Фитаты связывают пищевой цинк в нерастворимые соединения. Энтеропатический акродерматит сочетает в себе почти все нарушения тех важнейших функций, в которых участвует цинк. Это и хронические поносы (вследствие недостаточности пищеварительных ферментов и нарушения всасывания жиров), а вследствие этого вторичный дефицит большинства других важнейших нутриентов; нарушение роста (в первую очередь костей); сухость и ранимость кожи, гнойный дерматит, выпадение волос; нарушение ночного зрения и фотофобия; эмоциональная неустойчивость, раздражительность, мозжечковая атаксия; иммунодефицитные состояния.
Пища — несомненно, основной источник цинка. Содержание цинка в пищевых продуктах обычно колеблется в пределах 800…2500 мкг%. Однако в печени, мясе и бобовых оно достигает 3000–5000 мкг%. Суточная потребность в цинке 5–20 мг. Она вполне удовлетворяется обычным рационом. Среднесуточное поступление цинка только с питьевой водой составляет порядка 400 мкг. Иногда дефицит цинка может испытывать организм детей и подростков, которые недостаточно употребляют животные продукты.
Селен. Еще в середине XX в. селен не только не рассматривался наукой о питании, но даже считался очень токсичным элементом с канцерогенными свойствами. Однако уже в 1960-х гг. было установлено, что причиной эндемической кардиомиопатии у животных и людей (болезнь Кешана) является дефицит селена в почве. В 1970-е гг. свойства селена были всесторонне изучены и оказалось, что данный элемент необходим для активации одного из ключевых ферментов антиоксидантной системы организма — глутатионпероксидазы. Этот фермент предотвращает активацию перекисного окисления липидов мембран — процесса, который вызывает нарушение структурной и функциональной целостности мембран клеток, способствует повышению проницаемости и снижению устойчивости клеточных структур к повреждающим воздействиям.
Особенно страдает при недостатке селена сердечно-сосудистая система, что проявляется прогрессирующим атеросклерозом и слабостью сердечной мышцы, а в условиях хронического дефицита селена может развиваться практически неизлечимая кардиомиопатия. Кроме того, было показано, что селен является необходимым коферментом йодпероксидазы — основного фермента синтеза гормонов щитовидной железы, то есть дефицит селена может в значительной мере усугублять проявления йодной недостаточности, а назначение препаратов одного только йода может быть малоэффективным. В последнее время на уровне современных исследований находит подтверждение одно из важных наблюдений древнекитайской медицины, указывающее на то, что адекватное обеспечение организма селеном способствует замедлению процесса старения и ведет к долголетию. Интересно заметить, что знаменитые лечебные сорта зеленого чая, поставлявшиеся с целью достижения здоровья и долголетия в императорские дворцы в Древнем Китае, выращивались в тех горных провинциях, в почвах которых уже в настоящее время с помощью современных аналитических методов определяется высокое содержание селена.
После открытия селена было установлено, что витамин Е и селен действуют на разные звенья одного процесса и являются строго взаимодополняющими друг друга, то есть их антиокислительная активность при совместном применении резко возрастает. Синергизм обоих антиоксидантов особенно интересен в контексте противораковой активности. Так, было показано, что назначение препаратов селена одновременно с витамином Е значительно усиливало антиканцерогенный эффект в отношении экспериментальных опухолей. В связи с этим интересно отметить, что семена растений наряду с витамином Е также содержат значительные количества селена.
Поступление селена с пищей зависит от условий и характера потребления пищи и уровня содержания селена в пищевых продуктах. Овощи и фрукты являются в основном бедным источником поступления селена, в отличие от зерна, зерновых продуктов, мяса (особенно субпродуктов), продуктов моря, которые содержат существенные количества селена, обычно намного превышающие 0,2 мг/кг в пересчете на сырую массу. Химический состав почвы и содержание в ней селена существенно влияют на количество селена в зерне, варьирующее в пределах от 0,04 до 21 мг/кг.
Молибден. Общее количество молибдена в организме взрослого человека составляет порядка 7 мг. Содержание молибдена в крови составляет около 0,5 мкг на 100 мл. Более высокие концентрации этого элемента были обнаружены у людей, проживающих в регионах, где почва наиболее богата соединениями этого металла. Так, в некоторых районах Армении отмечены частые случаи заболевания подагрой у жителей, которые питаются в основном местными продуктами, в которых были обнаружены чрезвычайно высокие уровни молибдена. Содержание его в рационе питания жителей этого района составляло 10–15 мг. В других районах, где случаи подагры встречались реже, люди с пищей получали всего 1–2 мг молибдена в день.
Молибден является составной частью ряда ферментов, таких как ксантиноксидаза, альдегидоксидаза, сульфатоксидаза. Известно, что молибден тормозит развитие кариеса.
Предполагаемая дневная потребность в молибдене составляет 2 мкг на 1 кг массы тела. В России суточное потребление молибдена составляет 0,27 мг.
Наиболее богаты молибденом различные виды овощей (например, бобовые) и внутренние органы животных.
Кобальт. Биологическое действие кобальта известно с 1948 г., когда учеными Рикесом и Смитом было установлено, что атом кобальта является центральным в молекуле витамина B12. Максимальная концентрация кобальта в тканях равна около 100 мкг/кг. Общее содержание кобальта в организме взрослого человека составляет 5 мг. Человек с пищей ежедневно получает 5,63–7,94 мкг кобальта, из которых 73–97 % усваивается.
Средняя суточная потребность в кобальте составляет 60 мкг на 1 кг массы тела. Считают, что человек нуждается в кобальте только в виде цианокобаламина (витамин В12). В некоторых странах соединения кобальта применяли в качестве пищевой добавки к пиву для стабилизации пены.
Однако выяснилось, что такая добавка явилась причиной сердечных заболеваний у потребителей пива. Поэтому в настоящее время от использования соединений кобальта в виде пищевой добавки отказались.
3. Влияние технологической обработки на минеральный состав пищевых продуктов
При переработке пищевого сырья, как правило, происходит снижение содержания минеральных веществ (кроме случаев добавления пищевой соли). В растительных продуктах они теряются с отходами. Так, содержание ряда макро- и особенно микроэлементов при получении крупы и муки после обработки зерна снижается, так как в удаляемых оболочках и зародышах этих компонентов находится больше, чем в целом зерне. Сравнительный анализ минерального состава в пшеничной муке высшего сорта и муки из цельносмолотого зерна приведен ниже (содержание элементов указано в мг/100 г продукта):

Например, в среднем в зерне пшеницы и ржи зольных элементов содержится около 1,7 %, в муке же в зависимости от сорта от 0,5 (в высшем сорте) до 1,5 % (в обойной). При очистке овощей и картофеля теряется от 10 до 30 % минеральных веществ. Если их подвергают тепловой кулинарной обработке, то в зависимости от технологии (варка, обжаривание, тушение) теряется еще от 5 до 30 %.
Мясные, рыбные продукты и птица при отделении мякоти от костей в основном теряют такие макроэлементы, как кальций и фосфор.
При тепловой кулинарной обработке (варка, жарение, тушение) мясо теряет от 5 до 50 % минеральных веществ. Однако если обработку вести в присутствии костей, содержащих много кальция, то возможно увеличение содержания кальция в кулинарно обработанных мясных продуктах на 20 %.
В технологическом процессе за счет недостаточно качественного оборудования может переходить из него в конечный продукт некоторое количество микроэлементов. Так, при изготовлении хлеба при тестоприготовлении в результате контакта теста с оборудованием содержание железа может увеличиваться на 30 %. Этот процесс нежелательный, поскольку вместе с железом в продукт могут переходить и токсичные элементы, содержащиеся в виде примесей в металле. При хранении консервов в жестяных сборных (то есть спаянных) банках с некачественно выполненным припоем или при нарушении защитного лакового слоя в продукт могут переходить такие высокотоксичные элементы, как свинец, кадмий, а также олово.
Следует учесть, что ряд металлов, таких как железо и медь, даже в небольших концентрациях могут вызвать нежелательное окисление продуктов. Их каталитические окислительные способности особенно ярко проявляются в отношении жиров и жировых продуктов. Так, например, при концентрации железа выше 1,5 мг/кг и меди 0,4 мг/кг при длительном хранении сливочного масла и маргаринов эти металлы вызывают прогоркание продуктов. При хранении напитков в присутствии железа выше 5 мг/л и меди 1 мг/л при определенных условиях часто может наблюдаться их помутнение.
4. Обогащение продуктов питания минеральными веществами
Анализ литературных источников свидетельствует о том, что у различных групп населения России наряду с поливитаминным дефицитом наблюдается дефицит целого ряда макро- и микроэлементов, прежде всего кальция, железа, йода, а в некоторых регионах и селена.
Так, имеются данные по поступлению кальция с обычным рационом: для значительной части людей оно находится в пределах 200–500 мг в сутки, что намного меньше рекомендуемого уровня — 800–1000 мг для взрослых и 1200–1300 мг для подростков в период интенсивного роста. Дефицит кальция в суточных рационах иногда может достигать 40 %.
Что касается железа, то его дефицит чаще всего выявляется у детей, а также у женщин, в том числе беременных и кормящих грудью. Недостаток железа у беременных имеет место практически во всех регионах России.
Дефицит йода — один из наиболее распространенных в питании современного человека. Анализ питания различных групп населения свидетельствует о невозможности обеспечить рекомендуемые нормы потребления йода с помощью традиционных продуктов питания. Это связано с тем, что в последние годы существенно изменился характер питания населения, в частности в 3–4 раза снизился уровень потребления морской рыбы и морепродуктов, богатых йодом.
Основной причиной дефицита селена является его недостаточное поступление в организм людей, проживающих на территориях, где уровень этого элемента в почве, питьевой воде и сельскохозяйственной продукции местного производства низок. Такого рода дефицит может, по крайней мере частично, компенсироваться за счет межрегионального и международного товарообменов.
Один из путей ликвидации дефицита микронутриентов (в том числе минеральных веществ) — это регулярный дополнительный прием витаминно-минеральных препаратов или БАД, содержащих микронутриенты. Однако практика показывает, что прием таблеток или капсул малоприемлем для большей части людей, считающих себя здоровыми.
Составить же рацион с энергетической ценностью, не превышающей 2500–3000 ккал, который полностью удовлетворял бы потребность человека в витаминах и других незаменимых пищевых веществах, в частности макро- и микроэлементах, основываясь только на натуральных продуктах, практически невозможно.
Таким образом, проблема оптимальной обеспеченности населения микронутриентами в современных условиях оказывается неразрешимой традиционными методами и требует качественно новых подходов и решений.
Одним из путей, гарантирующих эффективное решение этой проблемы, по которому идут все передовые страны, является регулярное включение в рацион питания специализированных продуктов, обогащенных необходимыми микронутриентами.
В современных условиях для обогащения пищевых продуктов минеральными веществами чаще всего используют железо, кальций и йод, дефицит которых наиболее повсеместен и опасен.
Железо. Обогащение пищевых продуктов железом представляет собой сложную задачу как в технологическом, так и в гигиеническом отношении. Будучи металлом переменной валентности, железо легко катализирует окислительные процессы, в частности окисление аскорбиновой кислоты, и процессы перекисного окисления, ускоряя тем самым прогоркание жиров. Особенно активны в этом отношении легкоионизируемые, быстрорастворимые соли железа, то есть именно те его формы, которые в технологическом отношении были бы наиболее удобны для равномерного внесения железа в обогащаемые им продукты.
Плохорастворимые соли железа более безопасны, но менее удобны технологически, поскольку для их равномерного распределения по массе обогащаемого продукта необходимы более сложные в аппаратурном и технологическом отношении способы сухого смешивания.
Другую, не меньшую сложность представляет проблема биоусвояемости различных форм железа. Наиболее хорошо всасывается и усваивается организмом так называемое «гемовое» железо, входящее в состав гемоглобина и других гемовых соединений, присутствующих в мясных изделиях. Значительно хуже усваивается «негемовое» железо, входящее в состав различных неорганических и органических солей и находящееся в них в двухили трехвалентном состоянии. При этом необходимым условием всасывания «негемового» железа является его восстановление до двухвалентного состояния Fe(II), что достигается, в частности, при взаимодействии Fe(III) с аскорбиновой кислотой.
Еще одной трудностью, с которой сталкиваются производители обогащенных железом продуктов питания, является наличие во многих видах продовольственного сырья соединений — ингибиторов абсорбции железа, существенно снижающих биодоступность железа. К ним относятся прежде всего фитиновые соединения зерновых продуктов, соединения фенола, соли кальция и некоторые виды белков сои и молока.
Существуют различные пути уменьшения действия ингибиторов абсорбции железа. Наиболее часто для улучшения всасывания железа используется аскорбиновая кислота (витамин С), которая положительно влияет на усвоение как эндогенного, так и вносимого для обогащения железа. Кроме того, этот витамин снижает отрицательное действие на всасывание железа практически всех ингибиторов, в том числе кальция, фитиновой кислоты и полифенолов сои.
Принимая во внимание, что для успешного всасывания «негемовых» форм железа требуется аскорбиновая кислота, а для включения его в состав гемоглобина необходимы витамины В2, В6, В12 и фолиевая кислота, недостаток которых весьма распространен, то естественно, что обогащение продуктов питания железом должно сочетаться с их одновременным обогащением всеми этими жизненно важными микронутриентами путем применения соответствующих железосодержащих мультивитаминных премиксов, таких как «Ровифарин 955», «Ровифарин 4D», «Валетек-8» и т. п.
Кальций. Восполнение кальциевого дефицита и тем более достижение оптимальной обеспеченности организма этим элементом за счет обычных продуктов питания крайне затруднительно для людей, не переносящих молоко и молочные продукты, которые являются практически единственным, если не считать сои, более или менее богатым его источником.
Именно это обстоятельство настоятельно диктует необходимость создания пищевых продуктов, обогащенных столь важным макроэлементом. С этой целью добавки кальция обычно вводят в муку и хлебобулочные изделия. В последние годы широкое распространение получило обогащение кальцием плодовых соков и напитков на молочной основе, в частности йогуртов.
Для обогащения муки и хлебобулочных изделий чаще всего используют карбонат кальция или более дорогие фосфаты кальция, например трикальцийфосфат.
Для обогащения плодово-ягодных соков и напитков лучше использовать хорошо растворимый лактат кальция, недостатком которого является его относительно высокая цена и не очень большое содержание кальция.
В последнее время для обогащения плодовых соков с мякотью, молочных напитков (йогуртов) предлагается использовать специальные микронизированные формы плохорастворимых солей кальция, таких как трикальцийцитрат или трикальцийфосфат, которые, особенно в загущенных напитках, достаточно длительно находятся во взвешенном состоянии. Тем не менее такие напитки перед употреблением необходимо встряхивать, предупреждение о чем должно обязательно помещаться на этикетке.
Обогащение пищевых продуктов кальцием должно сочетаться с одновременным введением в них витаминов C, D, В2 и В6, которые необходимы для его успешного усвоения.
Йод. Для устранения дефицита йода широко используется йодированная соль. При выборе добавки для йодирования соли, как правило, учитывают физико-химические свойства соединения йода и чистоту самой соли. Так, например, широко использовавшийся ранее для йодирования соли KI является нестабильным веществом, он легко разрушается, особенно если соль хранится в условиях повышенной влажности и температуры, при воздействии кислорода воздуха и прямых солнечных лучей. Для повышения сохранности йода в этом случае использовались стабилизаторы (тиосульфат натрия, гидроксид кальция) и осушители (углекислый магний или углекислый кальций).
В настоящее время в большинстве стран мира, в том числе и в нашей стране, при обогащении соли и других продуктов йодом предпочтение отдается высокостабильному йодату калия (KIO3). Он устойчив к окислению и не требует дополнительного введения стабилизаторов. Поскольку KIO3 имеет меньшую растворимость, чем KI, он медленнее мигрирует из обогащенной соли в упаковочный материал.
Специалистами Института питания РАМН и ЗАО «Валетек Продимпекс» разработана высококачественная пищевая поваренная соль «Экстра», обогащенная йодатом калия до гарантированного содержания йода от 35 до 55 мкг на 1 г соли, имеющая практически неограниченный срок годности.
Наряду с производством этой соли ЗАО «Валетек Продимпекс» выпускает также соль профилактическую йодированную с пониженным содержанием натрия и обогащенную калием и магнием.
Обе эти соли с успехом используются для обогащения йодом хлебобулочных изделий и других продуктов питания, а также готовых блюд, в рецептуру которых входит поваренная соль.
5. Методы определения минеральных веществ
Для анализа минеральных веществ в основном используются физико-химические методы — оптические и электрохимические.
Практически все эти методы требуют особой подготовки проб для анализа, которая заключается в предварительной минерализации объекта исследования. Минерализацию можно проводить двумя способами: «сухим» и «мокрым».
«Сухая» минерализация предполагает проведение при определенных условиях обугливания, сжигания и прокаливания исследуемого образца.
«Мокрая» минерализация предусматривает еще и обработку объекта исследования концентрированными кислотами (чаще всего HNO3 и H2SO4).
5.1. Спектральные методы анализа
Фотометрический анализ (молекулярная абсорбционная спектроскопия). Он используется для определения меди, железа, хрома, марганца, никеля и других элементов. Метод абсорбционной спектроскопии основан на поглощении молекулами вещества излучений в ультрафиолетовой, видимой и инфракрасной областях электромагнитного спектра. Анализ можно проводить спектрофотометрическим или фотоэлектроколориметрическим методами.
Фотоэлектроколориметрия — анализ, основанный на измерении поглощения окрашенными растворами монохроматического излучения видимой области спектра. Измерения проводят с помощью фотоэлектроколориметров, снабженных узкополосыми светофильтрами. Если исследуемое вещество не окрашено, его необходимо перевести в окрашенное соединение, проведя химическую реакцию с определенными реагентами (фотометрическую аналитическую реакцию).
Спектрофотометрия — метод анализа, основанный на измерении поглощения монохроматического излучения в ультрафиолетовой, видимой и инфракрасной областях спектра. Такие измерения проводят с помощью спектрофотометров, где в качестве монохроматизаторов используются диспергирующие призмы и дифракционные решетки.
Количественный анализ исследуемого иона обычно проводят методом градуировочного графика.
Эмиссионный спектральный анализ. Методы эмиссионного спектрального анализа основаны на измерении длины волны, интенсивности и других характеристик света, излучаемого атомами и ионами вещества в газообразном состоянии. Эмиссионный спектральный анализ позволяет определить элементарный состав неорганических и органических веществ.
Интенсивность спектральной линии определяется количеством возбужденных атомов в источнике возбуждения, которое зависит не только от концентрации элемента в пробе, но и от условий возбуждения. При стабильной работе источника возбуждения связь между интенсивностью спектральной линии и концентрацией элемента (если она достаточно мала) имеет линейный характер, то есть в данном случае количественный анализ можно также проводить методом градуировочного графика.
Наибольшее применение в качестве источника возбуждения получили электрическая дуга, искра, пламя. Температура дуги достигает 5000–6000 °С. В дуге удается получить спектр почти всех элементов. При искровом разряде развивается температура 7000–10000 °С и происходит возбуждение всех элементов. Пламя дает достаточно яркий и стабильный спектр испускания. Метод анализа с использованием в качестве источника возбуждения пламени называют пламенно-эмиссионным анализом. Этим методом определяют свыше 40 элементов (щелочные и щелочно-земельные, Сu2+, Мn2+ и др.).
Атомно-абсорбционная спектроскопия. Метод основан на способности свободных атомов элементов в газах пламени поглощать световую энергию при характерных для каждого элемента длинах волн.
В атомно-абсорбционной спетроскопии практически полностью исключена возможность наложения спектральных линий различных элементов, так как их число в спектре значительно меньше, чем в эмиссионной спектроскопии.
Уменьшение интенсивности резонансного излучения в условиях атомно-абсорбционной спетроскопии подчиняется экспоненциальному закону убывания интенсивности в зависимости от толщины слоя и концентрации вещества, аналогичному закону Бугера–Ламберта–Бера:
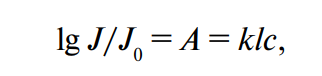
где J0 — интенсивность падающего монохроматического света; J — интенсивность прошедшего через пламя света; k — коэффициент поглощения; l — толщина светопоглощающего слоя (пламени); c — концентрация.
Постоянство толщины светопоглощающего слоя (пламени) достигается с помощью горелок специальной конструкции.
Методы атомно-абсорбционного спектрального анализа находят широкое применение для анализа практически любого технического или природного объекта, особенно в тех случаях, когда необходимо определить небольшие количества элементов.
Методики атомно-абсорбционного определения разработаны более чем для 70 элементов.
5.2. Электрохимические методы анализа
Ионометрия. Метод служит для определения ионов К+, Na+, Са2+, Мn2+, F–, I–, Сl — и т. д.
Метод основан на использовании ионоселективных электродов, мембрана которых проницаема для определенного типа ионов (отсюда, как правило, высокая селективность метода).
Количественное содержание определяемого иона проводится либо с помощью градуировочного графика, который строится в координатах Е—рС, либо методом добавок. Метод стандартных добавок рекомендуется использовать для определения ионов в сложных системах, содержащих высокие концентрации посторонних веществ.
Вольтамперометрия. Это электрохимические методы, основанные на изучении поляризационных кривых (вольтамперограмм), полученных в электролитической ячейке с поляризующимся индикаторным электродом и неполяризующимся электродом сравнения. К этим методам относят полярографию, инверсионную вольтамперометрию (ИВА) и амперометрическое титрование.
Современная вольтамперометрия — это высокочувствительный метод определения неорганических и органических соединений, один из наиболее универсальных методов определения следовых количеств веществ. Одним из достоинств этого метода является возможность одновременного определения нескольких элементов в смеси, а также то, что современные полярографы позволяют получить линейную зависимость тока от концентрации вещества в диапазоне 10–8–10–2 М.
Полярография. Метод переменно-токовой полярографии используют для определения токсичных элементов (ртуть, кадмий, свинец, медь, железо).
Метод основан на изучении вольтамперных кривых, полученных при электролизе электроокисляющегося или электровосстанавливающегося вещества. В качестве индикаторного электрода в полярографии чаще всего применяют ртутный капельный электрод, иногда твердые микроэлектроды — платиновый, графитовый. В качестве электрода сравнения используют либо ртуть, налитую на дно электролизера, либо насыщенный каломельный полуэлемент.
По мере увеличения напряжения наступает момент, когда все ионы, поступающие к электроду за счет диффузии, немедленно разряжаются и концентрация их в приэлектродном слое становится постоянной и практически равной нулю. Ток, протекающий в это время в цепи, называют предельным диффузионным током.
Количественный полярографический анализ основан на использовании прямой пропорциональной зависимости величины диффузионного тока от концентрации определяемого элемента.
Инверсионная вольтамперометрия. В отличие от полярографии, в этом методе обычно используется трехэлектродная электрохимическая ячейка: рабочий электрод–твердый графитовый электрод с амальгамированной поверхностью, вспомогательный электрод–графитовый, электрод сравнения–хлорсеребряный. На рабочем (индикаторном) электроде проходят электрохимические процессы (восстановления или окисления определяемых металлов). Вспомогательный электрод составляет с рабочим электрическую цепь. Потенциал рабочего электрода измеряют по отношению к электроду сравнения, потенциал которого постоянен и известен.